THE францій, символ Fr, атомний номер 87, є елементом, що належить до групи 1 Періодична таблиця, лужні метали. Однак, на відміну від інших елементів групи, францій не має стабільних ізотопів, що навіть ускладнило його відкриття. Насправді, францій був останній елемент, який потрібно відкрити та виділені в природних зразках.
Його велика атомна нестабільність не дозволяє отримувати видимі та важкі зразки, тому його фізико-хімічні властивості екстраполюються з даних інших лужних металів. Підраховано, що в земній корі всього 30 грамів францію, що робить його другий за рідкістю елемент на планеті, позаду лише астат.
Читайте також: Рубідій — елемент, що використовується при виготовленні спеціальних окулярів і атомних годин
резюме francium
Францій — лужний метал, розташований у сьомому періоді періодичної таблиці, символ Fr, Z = 87.
Він не має стабільних ізотопів і є другим за рідкістю елементом на планеті.
Його найстабільніший ізотоп має час півжиття 22 хвилини.
Це елемент з найбільшим атомний промінь періодичної таблиці, крім того, що є найбільш електропозитивним.
Його можна отримати лише ядерними процесами, його важко виділити.
Досі немає практичних застосувань, пов’язаних з францієм.
Властивості Francium
символ: о.
атомна маса: 223,02 грн.
Точка злиття: 22°C (приблизно).
Точка кипіння: 665 °C (оцінка).
Щільність: 2,5 г/см³ (приблизно).
електронегативність: 0,79.
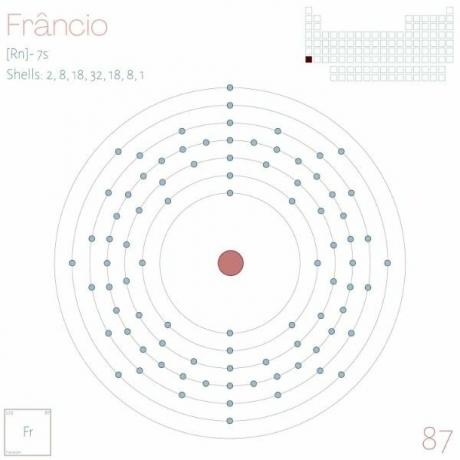
Електронний розподіл: [Rn] 7 с1.
→ Відеоурок про періодичні та аперіодичні властивості хімічних елементів
Характеристики Францію
францій має кілька ізотопів, але найстабільнішим є ізотоп 233, період напіврозпаду якого становить 22 хвилини. Лише ізотоп 212 має подібний період напіврозпаду 21 хвилину, тоді як інші навіть не наближаються до цього, а можуть навіть мати період напіврозпаду порядку секунд.

все це атомна нестабільність перешкоджає визначенню важливих фізичних характеристик і властивостей. Фактично відомі властивості були отримані в екстремальних умовах. розведення (концентрація порядку 10-15 моль/л).
Як лужного металу, його ступінь окиснення, як відомо, дорівнює +1. Експерименти також показали, що францій є найбільшим елементом електропозитивний періодичної таблиці. Інша лідируюча позиція, яку цей елемент займає в таблиці, - це елемент з найбільшим діаметром, з 2,7 ангстрем (10-10 м).
Як і інші лужні метали, францій залишається в розчині, тоді як інші елементи випадають в осад у вигляді гідроксидів, карбонатів, фторидів, сульфідів, хроматів тощо.
Читайте також: Що таке радіоактивні елементи?
Отримання францію
Найбільш стабільним ізотопом Fr був Францій-223 вперше виявлено через альфа-випромінювання актину-227. Також можна отримати францій (ізотоп 212) шляхом бомбардування золото (197Au) з киснем-18 (18О) в ядерному реакторі.
Францій можна отримати кількома способами. Наприклад, існує ймовірність його осадження цезій, через солі важкорозчинні елементи, такі як перхлорат (ClO4-), гексахлорплатинат (PtCl62-), йодат (IO4-), між іншими. Проте, як очікується, розділення цезію та франію буде дуже складним.
Інші методи, розроблені в 1960-х і 1970-х роках, дозволили відділення франію від розчинів цезію та рубідію через катіонообмінні смоли. Францій-223, який був відкритий в результаті альфа-випромінювання актинію-227, також можна відокремити від актинію та інших продуктів розпаду за допомогою методів селективного осадження. Існує також інший метод, який використовується з відносним успіхом: сублімація хлориду францію (FrCl) при температурі близько 300 °C.
Аплікації франція
Тести з щурами показали, що францій накопичується в нирках, печінці та слинних залозах. Крім того, була спроба застосувати його в ядерній медицині, в діагностиці раку, але труднощі в його підготовці та виділенні зробили проект нездійсненним. Ця характеристика, додана до його низького періоду напіврозпаду, робить францій один з небагатьох елементів без практичного застосування.
Однак факт наявності в найбільший атомний радіус періодичної системи і має лише один електрон в валентний шар він цікавить деяких дослідників його природою. У 2002 році групі дослідників у Сполучених Штатах вдалося захопити 300 000 атомів францію, щоб дізнатися більше про цей елемент.
Перегляньте наш подкаст: Твердий, як діамант: що це означає?
історія франція
Що виділяється в історії франціума, так це кількість разів, коли люди казали, що відкрили його після Менделєєв передбачив існування цього елемента в 1871 році, під імям ека-цезій.
Давно відомо, що після елемента 83, вісмуту, періодична система показує лише радіоактивні та нестабільні елементи — за винятком, наприклад, урану та торію. Незважаючи на це, це не завадило багатьом вченим шукати елемент 87 у природних джерелах і, найчастіше, заявляти про його відкриття.

Наприклад, У 1925 р. російський хімік Добросердов спостерігав слабку радіоактивність у зразку калій, дійшовши висновку, що це буде елемент 87, і назвавши його росії, на честь рідної країни. Проте найкращим поясненням цього факту було те, що насправді була виявлена радіоактивність ізотопу. 40K, бета-випромінювач, який становить близько 0,012% природного калію.
У 1926 році англійські хіміки Дрюс і Лорінг, аналізуючи спектральні лінії сульфату марганцю (II), вони також припускали спостерігати деякі лінії, що стосуються елемента 87, для якого вони пізніше запропонували ім'я луг. Однак слабкість доказів збентежила дослідників рухатися вперед.
Потім, у 1930 році, Фред Еллісон заявив про відкриття елемента 87 після деяких експериментів із зразками полуциту (руда, багата цезієм) і лепідоліт (руда з літій в його складі). Еллісон запропонувала назву virginium на честь американського штату Вірджинія. Однак у 1934 році Макферсон продемонстрував неточності у відкритті Еллісон.
Через два роки Жан Перрен, французький фізик, який, як відомо, підтвердив теорію броунівського руху Ейнштейна, зазначивши: Таким чином, достатні докази існування атомів приєдналися до римського фізика Хорія Хулубея в серії експериментів з променями X Потім вони отримали очікувані результати для елемента 87, який вони негайно назвали молдавій, щодо регіону Молдови, батьківщини Хулубея. Однак, знову ж таки, твір піддавався критиці у світлі інтерпретацій.
Ніхто з дослідників не міг зрозуміти, але те, що сталося, так це те, що францій має дуже нестабільні ізотопи з дуже коротким періодом напіврозпаду. Нещастя була така, що навіть розглядалося неіснування елемента 87.
Однак у 1939 році відкриття елемента 87 відбулося кимось, хто починав працювати лаборантом не хто інший, як Марія Кюрі, у Парижі: The Французька Маргарита Перей. Маючи гарний досвід роботи з радіоактивними зразками та їх очищення, Пері було доручено проаналізувати радіоактивний зразок актинію, елемент 89.
науковець був першим, хто спостерігав альфа- та бета-випромінювання актинія, відкриваючи новий елемент з періодом напіврозпаду 21 хвилину. Тоді француженка обережно повідомила про своє відкриття і в 1946 році захистила докторську дисертацію. Елемент 87: Актиній-К.
Потім новий елемент отримав назву францій на честь своєї рідної країни, спочатку із символом Фа. У 1949 році в Міжнародний союз чистої та прикладної хімії (Iupac) підтвердив елемент з назвою, даною Перей, але в 1951 році змінив символ на о.
Розв’язували вправи на франціум
питання 1
Францій (Fr, Z = 87) — лужний метал з коротким періодом напіврозпаду і нестабільний. Однак відомо, що він має деякі властивості, подібні до інших лужних металів.
На основі наведеної вище інформації, яка ймовірна сполука утворюється між францієм і бромом (Br, Z = 35)?
A) FrBr2
Б) о2бр
C) FrBr
D) FrBr3
Відповісти
Францій, як лужний метал, має NOX, що дорівнює +1. Вже бром, а галоген, за відсутності кисню має NOX, що дорівнює -1. Тому найбільш вірогідною сполукою серед них є буква C, FrBr.
питання 2
Радіус атома є надзвичайно важливою періодичною властивістю, оскільки вона не тільки розрізняє атоми за їх розмірами, але й допомагає зрозуміти реакційну здатність та інші властивості атомів.
Серед елементів періодичної таблиці найбільший атомний радіус має елемент:
А) Ф
B) Cs
В) Х
Г) о
E) Ог
Відповісти
Відомо, що атомний радіус тим більше, чим більше період елемента і менше число електрони у валентному шарі. Таким чином, елементом з найбільшим радіусом є францій Fr, оскільки він знаходиться в сьомому періоді періодичної системи і має лише один валентний електрон.
Стефано Араужо Новаїс
Вчитель хімії
