В реакції горіння вони присутні в багатьох аспектах нашого повсякденного життя. Наприклад, основні джерела виробництва енергії є результатом спалювання або спалювання деяких видів палива, таких як етанол, бензин, деревне вугілля тощо. Крім того, енергія, яка нам потрібна для виживання та виконання роботи, є результатом реакцій горіння, які відбуваються всередині наших клітин, коли ми «спалюємо» їжу, яку ми їмо.
Але що потрібно для реакції горіння?
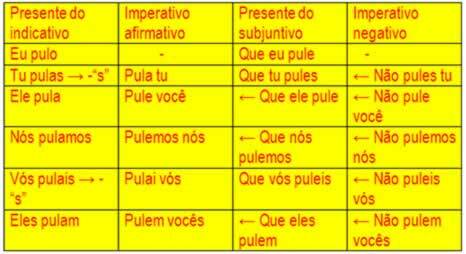
Потрібні три речі:
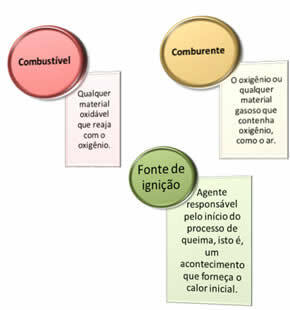
Ці три фактори складають трикутник вогню, тому що як тільки починається реакція горіння, енергія, що вивільняється, підтримує реакцію і дозволяє їй тривати до тих пір, поки не закінчиться паливо, окислювач або тепло (вивільнена енергія). Це означає, що буде a Ланцюгова реакція.
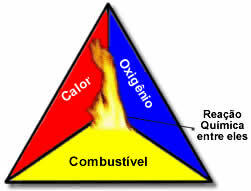
Наприклад, якщо хтось кине запалену сигарету в лісі, виникне пожежа (реакція горіння). У цьому випадку, Буш це паливо, О кисень, присутній у повітрі атмосферним є окислювач це сигарета було запалено джерело займання. Це горіння триватиме до тих пір, поки не буде усунений один з трьох факторів. Якщо пожежники кинуть воду, спека буде ліквідована. Але навіть якщо нічого не зробити, щоб зупинити це горіння, воно в якийсь момент закінчиться, тобто коли закінчиться паливо (ліс).
Як уже зазначалося, в цих реакціях виділяється тепло, тому горіння є екзотермічною реакцією. Однак цей тип реакції є неповним згорянням. Щоб зрозуміти чому, подивіться різницю між повним і неповним згорянням:
Повне згоряння:
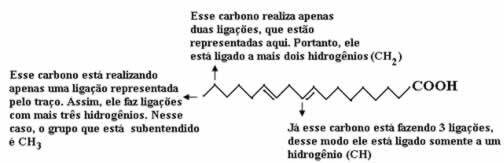
Аналізуючи органічні сполуки як паливо, ми повинні:
| THE повне згоряння це станеться, коли вуглецевий ланцюг розірватиметься і всі атоми вуглецю в вуглецевому ланцюгу повністю окисляться. |
| ти сформовані продукти вуглеводнями буде CO2 (вуглекислого газу) і Х2О (Вода). |
Спостерігайте повне згоряння ізооктану, який є одним із компонентів бензину.
Ç8Х18 (г) +25/2 О2 (г) → 8 CO2(g) +9 годин2О(1)
неповне згоряння
| У цьому випадку не вистачає окислювача, тобто достатньо кисню, щоб спалити все паливо. |
| Таким чином, утворені продукти є CO (чадний газ) і Х2О. |
Проте спостерігаємо те саме згоряння ізоктану, але тепер не повністю:
Ç8Х18 (г) + 17/2 О2(g) → 8 CO (g) +9 годин2О(1)
Прикладом є спалювання лісів, оскільки отримані викиди складаються з CO та певної речовини, такої як сажа (C), а також золи та інших простих і складних органічних сполук. Оксид азоту, озон і альдегіди також можуть утворюватися в результаті вторинних реакцій через наявність інших компонентів у повітрі.
Ç8Х18 (г) + 9/2 О2 (г) → 8С (g) +9 годин2О(1)
Автор: Дженніфер Фогаса
Закінчив хімію
Шкільна команда Бразилії
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/combustao-completa-incompleta.htm