О балансування рівняння дозволяє нам збігати кількість атомів, присутніх у хімічному рівнянні, таким чином, щоб воно стало істинним і являло собою хімічну реакцію.
Використовуйте наведені нижче запитання, щоб перевірити свої знання та перевірити відповіді, коментовані після зворотного зв’язку, щоб відповісти на ваші запитання.
питання 1
(Маккензі-СП)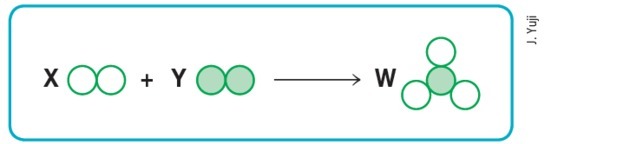
Якщо припустити, що порожнє та заповнене кола відповідно означають різні атоми, то схема вище буде представляти збалансовану хімічну реакцію, якщо замінити букви X, Y та W відповідно на значення:
а) 1, 2 і 3.
б) 1, 2 і 2.
в) 2, 1 і 3.
г) 3, 1 і 2.
д) 3, 2 і 2.
Альтернатива г) 3, 1 і 2.
1-й крок: Ми призначаємо літери, щоб полегшити розуміння рівняння.
2-й крок: ми додаємо індекси, щоб знати, хто має найбільше атомів у рівнянні.
| THE | |
| B |
А і В з’являються лише один раз у кожному члені рівняння. Однак, якщо скласти індекси, ми побачимо, що А має найвище значення. Тому ми розпочали балансування для нього.
3-й крок: Ми врівноважуємо елемент А, транспонуючи індекси та перетворюючи їх на коефіцієнти.
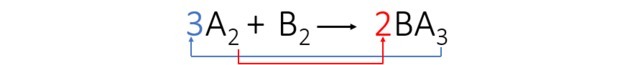
Ми спостерігали, що елемент В автоматично врівноважувався, а коефіцієнти рівняння становлять: 3, 1 і 2.
питання 2
(Unicamp-SP) Прочитайте наступне речення і перетворіть його у (збалансоване) хімічне рівняння, використовуючи символи та формули: „молекула газоподібного азоту, що містить два атоми азот на молекулу, реагує з трьома молекулами двоатомного газоподібного водню, утворюючи дві молекули газоподібного аміаку, який складається з трьох атомів водню і одного з азот ".
Відповідь:
Представляючи атоми, описані у питанні, ми можемо зрозуміти, що реакція відбувається наступним чином:
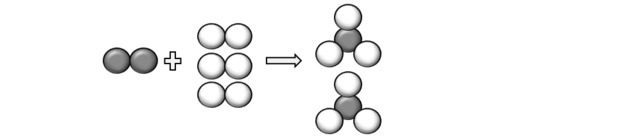
Отже, ми підійшли до рівняння:
питання 3
Перекис водню - це хімічна сполука, яка може розкладатися, утворюючи воду та кисень, згідно з хімічним рівнянням нижче.
Щодо цієї реакції, правильно збалансоване рівняння має вигляд:
а) Н2О2 → The2 + Н2О
б) 2 год2О2 → The2 + 2Н2О
в) Н2О2 → 2O2 + Н2О
г) 2 год2О2 → 2O2 + 2Н2О
Правильна альтернатива: б) 2Н2О2 → The2 + 2Н2О
Зверніть увагу, що перекис водню - це хімічна речовина, що складається з атомів двох хімічних елементів: водню та кисню.
Після реакції розкладання ви повинні мати однакову кількість атомів двох елементів як у реагентах, так і в продуктах. Для цього нам потрібно збалансувати рівняння.
Зверніть увагу, що ми маємо 2 атоми водню в реагенті (H2О2) і два атоми у продукті (H2О). Однак кисень має два атоми в реагенті (H2О2) і три атоми в продуктах (H2О і О2).
Якщо ми поставимо коефіцієнт 2 перед перекисом водню, ми подвоїмо кількість атомів в елементах.
Зверніть увагу, що якщо ми покладемо однаковий коефіцієнт разом із формулою для води, ми отримаємо однакову кількість атомів з обох сторін.
Отже, правильно збалансоване хімічне рівняння дорівнює 2Н2О2 → The2 + 2Н2О.
питання 4
(UFPE) Розглянемо хімічні реакції нижче.
Можна сказати, що:
а) всі врівноважені.
б) 2, 3 і 4 збалансовані.
в) збалансовані лише 2 і 4.
г) лише 1 є незбалансованим.
д) жоден не є правильно збалансованим, оскільки фізичний стан реагентів та продуктів різний.
Альтернатива б) 2, 3 і 4 збалансовані.
Варіанти 1 і 5 неправильні, оскільки:
- Рівняння 1 є незбалансованим, правильним балансом буде:
- Рівняння 5 є неправильним, оскільки сполукою, що утворюється в реакції, буде Н2ТІЛЬКИ3.
Для формування H2ТІЛЬКИ4 слід включати в рівняння окислення SO2.
питання 5
(Mackenzie-SP) Нагрітий до 800 ° C, карбонат кальцію розкладається на оксид кальцію (первинне вапно) та вуглекислий газ. Правильно збалансованим рівнянням, яке відповідає описуваному явищу, є:
(Дано: Ca - лужноземельний метал.)
Альтернатива c)
Кальцій - це лужноземельний метал, і для стабільності кальцію потрібно 2 електрона (Ca2+), що є зарядом кисню (O2-).
Таким чином, атом кальцію зв'язується з атомом кисню, і сполука, що утворюється, є СаО, що є негашеним вапном.
Інший продукт - вуглекислий газ (CO2). Обидва вони утворені карбонатом кальцію (CaCO3).
Поклавши це у рівняння:
Зауважимо, що кількості атомів уже правильні і не потребують збалансування.
питання 6
(UFMG) Рівняння не є збалансованим. Балансуючи його з найменшими можливими числами, сума стехіометричних коефіцієнтів буде такою:
а) 4
б) 7
в) 10
г) 11
д) 12
Альтернатива д) 12
Використовуючи пробний метод, порядок балансування буде таким:
1-й крок: Оскільки елементом, який з’являється лише один раз у кожному члені та має найвищий показник, є кальцій, ми почали балансувати для нього.
2-й крок: Ми стежимо за балансуванням радикального PO43-, який також з’являється лише один раз.
3-й крок: ми врівноважуємо водень.
При цьому ми спостерігаємо, що автоматично регулювалася кількість кисню і баланс рівняння:
Пам'ятаючи, що коли коефіцієнт дорівнює 1, вам не потрібно писати його в рівняння.
Додавши коефіцієнти, ми маємо:
питання 7
Горіння - це вид хімічної реакції, при якій енергія виділяється у вигляді тепла.
При повному згорянні речовини, утвореної вуглецем та воднем, утворюються вуглекислий газ та вода.
Поспостерігайте за реакціями горіння вуглеводнів і дайте відповідь, яке з рівнянь нижче неправильно збалансоване:
а) СН4 + 2O2 → CO2 + 2Н2О
б) С3H8 +502 → 3CO2 + 4Н2О
в) С4H10 + 13 / 3O2 → 4CO2 + 5 год2О
г) С2H6 + 7 / 2O2 → 2CO2 + 3Н2О
Неправильна відповідь: в) В4H10 + 13 / 3O2 → 4CO2 + 5 год2О
Щоб збалансувати хімічні рівняння, давайте спочатку розглянемо, який елемент з’являється лише один раз у кожному члені рівняння.
Зверніть увагу, що вуглець та водень утворюють лише один реагент та один продукт у кожному представленому рівнянні.
Тож давайте почнемо балансувати з воднем, оскільки він має більшу кількість атомів.
Отже, порядок балансування буде таким:
- Гідроген
- Вуглець
- Кисень
Гідроген
Оскільки продукт має 2 атоми водню, ми вставляємо число як коефіцієнт, помножений на 2, дає результат число атомів водню реагенту.
а) СН4 + O2 → CO2 + 2H2О
б) С3H8 + O2 → CO2 + 4H2О
в) С4H10 + O2 → CO2 + 5H2О
г) С2H6 + O2 → CO2 + 3H2О
Вуглець
Врівноваження здійснюється шляхом транспортування індексу вуглецю в реагент і використання його як коефіцієнта на продукті, що має атоми цього елемента.
а) СН4 + O2 → 1CO2 + 2Н2О
б) С3H8 + O2 → 3CO2 + 4Н2О
в) С4H10 + O2 → 4CO2 + 5 год2О
г) С2H6 + O2 → 2CO2 + 3Н2О
Кисень
Додаючи кількість атомів кисню в утворених продуктах, ми знаходимо кількість атомів елемента, який повинен реагувати.
Для цього ми повинні поставити як коефіцієнт число, помножене на 2, призводить до кількості атомів кисню в продуктах.
а) СН4 + O2 → 1CO2 + 2Н2О
2x = 2 + 2
2x = 4
х = 2
Тож правильним рівнянням є: СН4 + 2О2 → 1CO2 + 2Н2О.
б) С3H8 + O2 → 3CO2 + 4Н2О
2x = 6 + 4
2x = 10
х = 5
Тож правильне рівняння: C3H8 + 5О2 → 3CO2 + 4Н2О
в) С4H10 + O2 → 4CO2 + 5 год2О
2x = 8 + 5
2x = 13
x = 13/2
Тож правильне рівняння: C4H10 + 13/2О2 → 4CO2+ 5 год2О
г) С2H6 + O2 → 2CO2 + 3Н2О
2x = 4 + 3
2x = 7
x = 7/2
Тож правильне рівняння: C2H6 + 7/2О2 → 2CO2 + 3Н2О
Правильно збалансованими рівняннями є:
а) СН4 + 2O2 → CO2 + 2Н2О
б) С3H8 +502 → 3CO2 + 4Н2О
в) С4H10 + 13 / 2O2 → 4CO2 + 5 год2О
г) С2H6 + 7 / 2O2 → 2CO2 + 3Н2О
Таким чином, альтернатива в) С4H10 + 13 / 3O2 → 4CO2 + 5 год2Справа в тому, що він не має правильного балансу.
питання 8
(Enem 2015) Вапняки - це матеріали, що складаються з карбонату кальцію, які можуть виступати сорбентами для діоксиду сірки (SO2), важливий забруднювач повітря. Реакціями, що беруть участь у процесі, є активація вапняку шляхом прожарювання та фіксація SO2 з утворенням солі кальцію, що ілюструється спрощеними хімічними рівняннями.
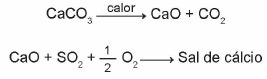
Враховуючи реакції, що відбуваються в цьому процесі десульфуризації, хімічна формула солі кальцію відповідає:
Альтернатива b)
Оскільки реакція збалансована, атоми в реагентах повинні мати однакову кількість продуктів. Таким чином,
Утворена сіль складається з:
1 атом кальцію = Ca
1 атом сірки = S
4 атоми кисню = O4
Отже, хімічна формула солі кальцію відповідає CaSO4.
питання 9
(UFPI) Реакція X з Y показана нижче. Визначте, яке рівняння найкраще представляє збалансоване хімічне рівняння.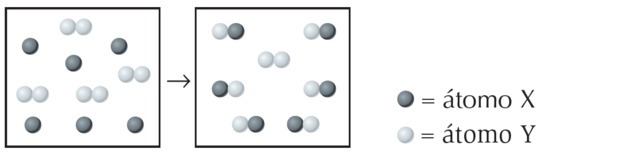
Альтернатива а)
На малюнку ми спостерігаємо, що вид X - це один атом, тоді як Y - двоатомний, тобто він утворюється шляхом з’єднання 2 атомів. Тож X реагує з Y2.
Сформований добуток представлений XY, при цьому рівняння є незбалансованим:
Ми збалансуємо рівняння наступним чином:
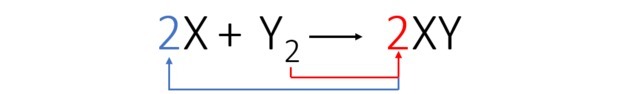
Відповідно до збалансованого рівняння, на малюнку нижче показано, як відбувається реакція та її частка.
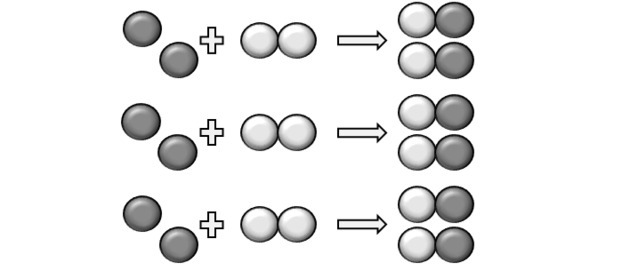
Для того, щоб відбулася реакція, має бути фіксоване співвідношення, і тому деяка сполука може не реагувати. Це те, що показано на малюнку, тому що в добутку ми бачимо, що Y2 не реагував.
питання 10
(Enem 2010) Мобілізація для сприяння кращій планеті для майбутніх поколінь стає все частішою. В даний час більшість засобів масового транспорту живляться за рахунок спалення викопного палива. Як приклад тягаря, спричиненого цією практикою, досить знати, що автомобіль виробляє в середньому близько 200 г вуглекислого газу на пройдений км.
Журнал «Глобальне потепління». 2, 8 рік. Публікація Instituto Brasileiro de Cultura Ltda.
Однією з основних складових частин бензину є октан (C8H18). Завдяки згорянню октанової енергії можливо, що дозволяє машині почати рух. Рівняння, яке представляє хімічну реакцію цього процесу, демонструє, що:
а) при цьому виділяється кисень у вигляді О2.
б) стехіометричний коефіцієнт для води становить 8 до 1 октану.
в) в процесі відбувається споживання води, завдяки чому виділяється енергія.
г) стехіометричний коефіцієнт для кисню становить 12,5 до 1 октану.
д) стехіометричний коефіцієнт для вуглекислого газу становить 9 до 1 октану
Альтернатива г) стехіометричний коефіцієнт для кисню становить 12,5 до 1 октану.
При балансуванні рівняння знаходимо такі коефіцієнти:
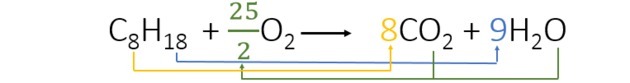
- Ми розпочали балансування воднем, який з’являється лише один раз у кожному елементі та має вищий показник. Оскільки є 18 атомів водню, що реагують, у продукті є 2, тому нам потрібно додати число, помножене на 2, дає 18. Отже 9 - коефіцієнт.
- Потім додаємо коефіцієнт 8 перед CO2 мати 8 атомів вуглецю в кожному елементі рівняння.
- Нарешті, просто додайте кількість кисню в продукті і знайдіть значення, помножене на 2, дає нам 25 атомів кисню. Отже, ми вибрали 25/2 або 12,5.
Таким чином, на спалювання 1 октану витрачається 12,5 кисню.
питання 11
(Fatec-SP) Суттєвою характеристикою добрив є їх розчинність у воді. Тому промисловість добрив перетворює фосфат кальцію, розчинність якого у воді дуже низька, у значно розчиннішу сполуку, яка є суперфосфатом кальцію. Цей процес представлений рівнянням:
де значення x, y та z складають відповідно:
а) 4, 2 і 2.
б) 3, 6 і 3.
в) 2, 2 і 2.
г) 5, 2 і 3.
д) 3, 2 і 2.
Альтернатива д) 3, 2 і 2.
Використовуючи алгебраїчний метод, ми формуємо рівняння для кожного елемента і прирівнюємо кількість атомів у реагенті до кількості атомів у продукті. Тому:
Збалансоване рівняння:
питання 12
Збалансуйте наведені нижче рівняння, використовуючи пробний метод.
Відповідь:
Рівняння складається з елементів водню та хлору. Ми збалансуємо елементи, просто додавши коефіцієнт 2 перед продуктом.
Рівняння не потрібно було збалансувати, оскільки кількості атомів вже скориговані.
Фосфор має два атоми в реагентах, тому, щоб збалансувати цей елемент, ми регулюємо кількість фосфорної кислоти в продукті до 2H3ПИЛ4.
Після цього ми спостерігали, що водень має 6 атомів у продукті, ми збалансували кількість цього елемента, додаючи коефіцієнт 3 до реагенту, який його містить.
На попередніх етапах кількість кисню була фіксована.
Розглядаючи рівняння, ми бачимо, що кількість водню та брому в продуктах удвічі більша якщо є в реагентах, то ми додаємо коефіцієнт 2 до HBr, щоб збалансувати ці два елементів.
Хлор має 3 атоми у продуктах і лише 1 у реагентах, тому ми балансуємо, ставлячи коефіцієнт 3 перед HCl.
Водень мав 3 атоми в реагентах і 2 атоми в продуктах. Для регулювання величин ми перетворюємо індекс Н2 в коефіцієнті ми множимо на 3, яке вже було в HCl, і отримуємо результат 6HCl.
Ми регулюємо кількість хлору в продуктах, щоб мати також 6 атомів і отримуємо 2AlCl3.
Алюміній мав у продуктах 2 атоми, ми відрегулювали кількість в реагентах до 2Al.
Ми балансуємо кількість водню в продукті до 3H2 і ми підбираємо кількість 6 атомів цього елемента в кожен член рівняння.
У рівнянні нітратний радикал (NO3-) має індекс 2 у продукті, ми перетворюємо індекс на коефіцієнт у реагенті для 2AgNO3.
Кількість срібла потрібно було відкоригувати, оскільки воно зараз має 2 атоми в реагентах, тому в продукті ми маємо 2Ag.
У реагентах ми маємо 4 атоми водню, і для збалансування цього елемента ми додаємо коефіцієнт 2 до продукту HCl.
Хлор тепер містить 4 атоми у продуктах, тому ми регулюємо кількість в реагенті до 2Cl2.
У нас в реагентах 6 атомів водню, і, щоб збалансувати цей елемент, ми регулюємо кількість води до 3H2О.
У нас в реагентах є 2 атоми вуглецю, і, щоб збалансувати цей елемент, ми регулюємо кількість вуглекислого газу до 2CO2.
Кисень повинен мати 7 атомів у реагентах, і, щоб збалансувати цей елемент, ми регулюємо кількість молекулярного кисню до 3O2.
Дивлячись на рівняння, нітратний радикал (NO3-) має індекс 2 у товарі. Ми перетворюємо індекс на коефіцієнт 2 в реагенті AgNO3.
У нас в реагентах є 2 атоми срібла, і для збалансування цього елемента ми регулюємо кількість хлориду срібла в продукті до 2AgCl.
У продукті є 3 атоми кальцію, і для збалансування цього елемента ми регулюємо кількість нітрату кальцію в реагенті до 3Ca (NO3)2.
Тоді у нас залишається 6 НІ радикалів3- в реагентах і, щоб збалансувати цей радикал, ми регулюємо кількість азотної кислоти в продуктах до 6HNO3.
Зараз у продуктах 6 атомів водню, і для збалансування цього елемента ми регулюємо кількість фосфорної кислоти в реагенті до 2H3ПИЛ4.
Дізнайтеся більше про розрахунки за допомогою хімічних рівнянь за адресою:
- Балансування хімічних рівнянь
- Стехіометрія
- Стехіометричні розрахунки
- Вправи на стехіометрію
- Вправи на періодичній системі