О Діаграма фаз це графік, який дозволяє визначити, в якому агрегатному стані знаходиться речовина у будь-який момент часу, знаючи її температуру та тиск.
Лабораторні вимірювання використовуються для побудови фазової діаграми даної речовини.
Діаграма поділена на три області, які представляють твердий, рідкий та паровий стан.
Крапки на лініях, які розмежовують ці області, позначають значення температури і тиску, що речовина може знаходитись у двох станах.
Фазова діаграма має такі елементи:
- крива Злиття: розділяє області, що відповідають твердому та рідкому станам.
- крива випаровування: розділяє ділянки, що відповідають рідкій та паровій фазам.
- крива сублімація: розділяє ділянки, що відповідають твердій та паровій фазам.
- потрійний бал: точка перетину трьох кривих (плавлення, випаровування та сублімація). Ця точка вказує на значення температури і тиску, які речовина може одночасно знаходитись у трьох станах.
- Критичний момент: вказує на найвищу температуру речовини, що є парою. З цього моменту вже неможливо розрізнити рідкий та паровий стан. При температурі вище критичної точки речовина стає газом.
На малюнку нижче ми представляємо представлення фазової діаграми:

Детальніше читайте на: Зміни фізичного стану.
крива плавлення
Речовини, як правило, збільшуються в обсязі, коли вони піддаються плавленню і, навпаки, зменшуються в обсязі, коли вони застигають. Як наслідок, збільшення тиску призводить до збільшення температури плавлення (температури плавлення).
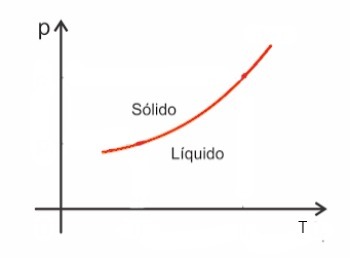
Однак є деякі винятки серед них вода, яка при таненні зменшується в обсязі. У цьому випадку збільшення тиску спричинює зменшення температури плавлення.
Таким чином, крива плавлення цих речовин буде виглядати так:
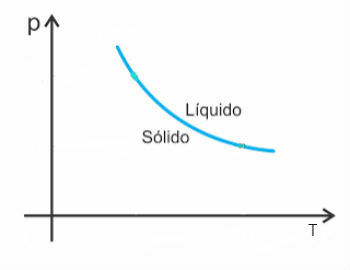
Приклад
Розглянемо фазову діаграму СО2 (вуглекислий газ), представлений нижче, і дайте відповіді на запитання:
а) Якою фазою є CO2 , коли ваша температура -60 ° C, а тиск 50 атм?
б) Певна кількість СО2 рідина піддається тиску 56 атм і утримується в контейнері. Якщо рідина нагрівається, підтримуючи постійний тиск, якою буде температура, при якій відбуватиметься випаровування?
в) Яке значення температури і тиску потрійної точки СО2?
г) Шматок сухого льоду (CO2) піддається тиску 2 атм. Він нагрівається, підтримуючи постійний тиск. У певний момент починає відбуватися зміна фази. Як називається ця зміна?
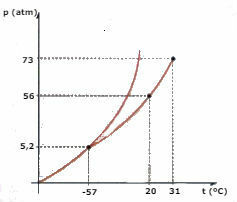
Дозвіл:
а) Спостерігаючи за діаграмою, робимо висновок, що CO2 буде в твердій фазі.
б) Випаровування відбуватиметься, коли температура досягне 20 ° С.
в) Потрійна точка відповідає перетину трьох кривих у випадку CO2, коли вона має температуру -57 ° С і тиск 5,2 атм, три фізичні стани можуть співіснувати.
г) Відбудеться сублімація
Щоб дізнатись більше, читайте також:
- Затвердіння
- Температура плавлення і кипіння
- Випаровування
- Конденсація
Розв’язані вправи
1) Енем - 2000
Навіть сьогодні дуже часто люди використовують глиняні ємності (ривки або неглазуровані керамічні горщики) для економії води при температурі, нижчій від температури навколишнього середовища. Це відбувається тому:
а) глина ізолює воду від навколишнього середовища, завжди підтримуючи її при нижчій температурі, ніж її власна, ніби це пінополістирол.
б) глина здатна «заморожувати» воду завдяки своєму хімічному складу. У реакції вода втрачає тепло.
в) глина пориста, пропускаючи через неї воду. Частина цієї води випаровується, забираючи тепло з морінга, а решта води, яка потім охолоджується.
г) глина пориста, що дозволяє воді осідати на зовнішній стороні глечика. Зовнішня вода завжди має вищу температуру, ніж внутрішня.
д) Морінга - це свого роду природний холодильник, що виділяє гігроскопічні речовини, які природним чином знижують температуру води.
Альтернатива c: глина пориста, що пропускає воду. Частина цієї води випаровується, забираючи тепло з морінга, а решта води, яка потім охолоджується.
2) Іта - 2013 рік
Розглянемо гіпотетичну фазову діаграму, схематично представлену на наступному малюнку:

Що представляють точки A, B, C, D та E?
точка А: точка сублімації
точка Б: потрійна точка
Точка С: точка плавлення / затвердіння
точка D: точка випаровування / конденсації
точка Е: критична точка
3) UECE - 2009
Дивлячись на діаграму фаз ПТ, показану нижче. Можна правильно зробити висновок, що речовина, яка пройшла процес сублімації, рухається по траєкторії:

а) X або Y
б) Y або U
в) U або V
г) Т або Х
Альтернатива b: Y або U
