Галоген - це органічна сполука, яка має принаймні один атом галогену. - тобто хімічні елементи з сімейства 17 або VII періодичної таблиці (F, Cl, Br, I або загалом: X) - приєднаний до групи, отриманої з вуглеводню.
RX (де X = F, Cl, Br або I)
Деякі галогеніди показані нижче:

Йод є найбільш реакційноздатним з усіх, а фтор найменшим, оскільки енергія зв’язку між галогеном та вуглецем зростає від напрямку йоду до фтору.
Інший момент полягає в тому, що реактивність також збільшується в цьому сенсі:

Таким чином, ця реакційна здатність відбувається з більшою легкістю у третинних галогенидах вуглецю завдяки характеру, який набуває вуглець, пов'язаний з органічним галогенідом:

Таким чином, група-заступник, така як ОН, яка буде утворювати спирт, сильніше притягується до третинного вуглецю, який має позитивний характер (1+), і заміщення стає простішим.
Галогеніди можуть зазнавати реакцій, які дозволяють отримувати практично всі інші органічні функції (алкоголь, ефір, алкін, ціанід або нітрил, амін тощо). Однак на практиці це нездійсненно, оскільки галогеніди є дуже дорогими сполуками.
Наприклад, для утворення спирту галогенід реагує з сильним підставою, таким як гідроксид натрію, у водному середовищі. Побачимо приклад нижче, в якому із лужного гідролізу етилхлориду (хлороетану) утворюється етанол:
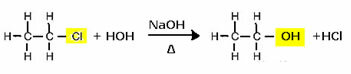
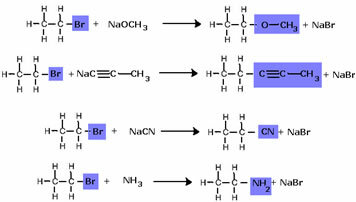
Зазначимо, що галогенідну групу замінив ОН, алкогольною функціональною групою. За тією ж схемою дотримуються утворення інших груп, диференціюючи лише реагент:
Дженніфер Фогача
Закінчив хімію
Шкільна команда Бразилії
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/reacoes-substituicao-haletos-organicos.htm