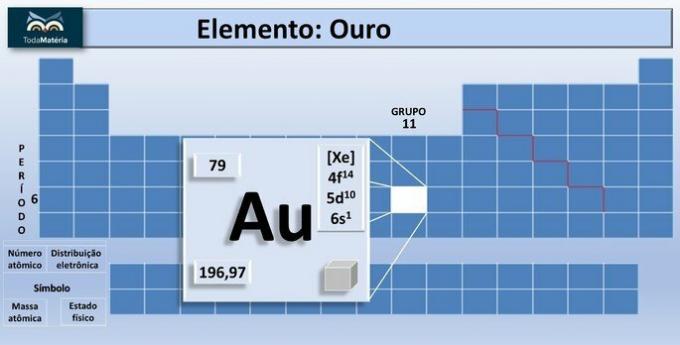
Золото - хімічний елемент у Періодичній системі, представлений символом Au, атомний номер якого становить 79 і належить до перехідних металів.
Це один з перших металів, якими маніпулювала людина, завдяки тому, що він виявляється чистим у природі.
Золото, як благородний метал, є одним з найбільш бажаних металів і широко використовується у виробництві ювелірних виробів, монет та декоративних предметів у вигляді сплаву з іншими металами.
Золоті особливості
- Має яскраво-жовтий колір
- Він стійкий до корозії
- Зустрічається вільно в природі у вигляді самородків або зерен
- М'який і гнучкий метал
- У природі мало багато
властивості золота
Золото має багато застосувань завдяки своїм властивостям, які виходять за межі його яскравості та кольору. Це метал, який легко обробляти та формувати, а отже, людина використовувала його довгий час.
Фізичні властивості
| Електропровідність | 45,2 х 106 S / m |
|---|---|
| Щільність | 19,3 г / см3 |
| Жорсткість | 2,5 (шкала Мооса) |
| Точка плавлення | 1064 ° С |
| Точка кипіння | 2856 ° С |
Хімічні властивості
| електронегативність | 2,54 |
|---|---|
| Енергія іонізації | 9,226 еВ |
| Число окислення (Nox) | +1, +3 |
| Реактивність |
Страждає від окислення:
|
| Найпоширеніші сполуки |
|
Походження золота
Завдяки своїм характеристикам записи про розвідку золота людиною сягають 6000 років. У Біблії можна побачити використання золота як символу багатства, а єгипетські ієрогліфи датують використання золота 4000 р. До н. Ç.
Цей метал пов’язаний з культурою та історією багатьох народів, оскільки його виявляли різні групи в різних місцях та часах.
У давнину є відомості про розвідку золота в Судані, північній Греції, Ірані та Китаї.
У середні віки, крім відкриття цього металу в інших місцях, таких як Австрія та Саксонія, рух назвав Алхімія, який прагнув перетворити звичайні метали у високоцінні матеріали, такі як золото.
Починаючи з XI століття, можна помітити експансію цього металу по всьому світу, що набуває широкого застосування в монетах.
Навіть в Америці, після його відкриття, було помічено, що люди, що мешкають у деяких регіонах, таких як інки та ацтеки, володіли запасами розвідки не тільки цього металу, але й срібла, що призвело до швидкої експлуатації іспанців у континент.
У Бразилії в регіонах Мінас-Жерайс, Мато-Гросу та Гояс були виявлені золоті шахти, що призвело до того, що "золота лихоманка" стала економічною діяльністю в колоніальній фазі країни.
Для чого потрібне золото?

Ювелірні вироби
Найбільше споживання золота - на виготовлення ювелірних виробів. Колір, блиск, довговічність та традиції використання цього металу роблять коштовність, що містить золото, цінною.
Для підвищення міцності матеріалу ремісники готують сплав з іншими металами, такими як платина, срібло та мідь.
Карат був розроблений для визначення кількості золота в сплаві. Наприклад: 24-каратне золото (24K) - це чисте золото, тоді як 12-каратне золото (12K) - це сплав, у якому 50% його складу належить цьому металу.
Монети
Золото здавна мало комерційну цінність і використовується як засіб обміну або грошей. Це пов’язано з його рідкістю, високою вартістю та можливістю бути фракціонованим.
Перші золоті монети були виготовлені в 560 р. До н. Ç. за наказом короля Лідії Креза (область сучасної Туреччини).
Існують також золоті злитки, які досі залишаються формою інвестування деякими установами через їхню простоту обробки та зберігання.
Електроніка
Оскільки воно стійке до корозії та має високу провідність, золото використовується в електроніці, яка використовує дуже низькі струми та напруги, що забезпечує надійність матеріалу.
Складні електронні пристрої, такі як стільникові телефони, GPS (глобальна система позиціонування) та калькулятори, мають у своєму складі невелику кількість золота.
Дізнайтеся більше про таблицю Менделєєва та інші хімічні елементи на:
- Періодична таблиця
- Хімічні елементи
- Сім'ї періодичної системи
- Історія періодичної системи