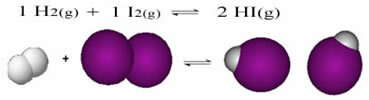
Окислення - це хімічна реакція, при якій атоми, іони або молекули втрачають електрони. Це також спричинює збільшення кількості окислення (nox).
Термін окислення спочатку був створений для позначення реакцій, в яких реагентом був кисень. Однак було встановлено, що в деяких випадках вони відбувалися за відсутності цього елемента. Оскільки цей термін був уже широко відомий, він продовжував застосовуватися.
Реакції окислення відбуваються одночасно з реакціями відновлення. Тому їх називають окисно-відновними, в яких переносяться електрони.
У окисно-відновних реакціях окислювач є тим, який приймає електрони, зазнаючи відновлення. Відновник втрачає електрони і зазнає окислення.
Приклади окислення
Окислення заліза
Іржа - це окислення заліза. Всі метали можуть зазнати окислення. Це відбувається внаслідок контакту металів з повітрям і водою. Спочатку корозія що є зносом металу внаслідок окислення. Потім він утворює іржа.
Див. Реакцію окисно-відновний для утворення іржі:
- Fe (и) → Fe2+ + 2e-. На цій стадії залізо втрачає два електрони, зазнає окислення
- О2 + 2 год2O + 4e- → 4OH-. O зменшення2
- 2Fe + O2 + 2Н2O → 2 Fe (OH)2. Загальне рівняння - Fe (OH)2 є гідроксидом заліза, відповідальним за коричневий колір іржі.
Для захисту заліза та сталі від окислення може бути використана техніка цинкування. Він складається з металевого цинкового покриття. Однак це дорогий процес, що в деяких випадках робить його нездійсненним.
Таким чином, корпуси кораблів і металеві платформи отримують металеві блоки магнію, що перешкоджають окисленню заліза. Магній вважається жертовним металом і його потрібно час від часу замінювати, коли він зношується.
Фарбування також може захистити метал від окислення, але це не настільки ефективно.

Іржа
Також читайте про Нержавіюча сталь і Сплави металів.
Окислення в органічній хімії
На додаток до металів, окислення може також відбуватися з Вуглеводні, особливо алкени. Органічне окислення має чотири форми: горіння, озоноліз, м’яке окислення та окислення енергії.
Горіння
THE горіння це хімічна реакція речовини з киснем, яка завершується утворенням світла та тепла. Кисень називають окислювачем. Речовина з вуглецем є паливом.
Кисень має функцію окислення палива, він є окисником горіння.
Горіння може бути повним або неповним. Знайте різницю між двома способами:
- Повне згоряння: Виникає при достатньому надходженні кисню. В кінці реакції діоксид вуглецю (CO2) і води (H2О).
- Неповне згоряння: Недостатньо подачі кисню, вони утворюються окис вуглецю (CO) та води (H2О).
Озоноліз
При такому типі реакції озон є реагентом, який призводить до окислення алкенів. Відбувається розрив подвійного зв'язку алкенів і утворення карбонільних сполук, таких як альдегіди і кетони.
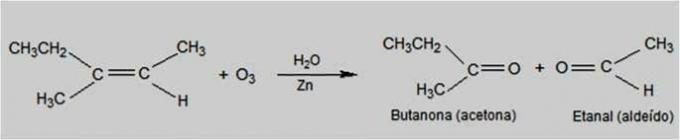
Реакція озонолізу
слабке окислення
Помірне окислення відбувається, коли окислювачем є така сполука, як перманганат калію (KMnO4), присутній у водному розчині, розведеному та охолодженому, нейтральному або слабоосновному.
Цей тип окислення відбувається за допомогою тесту Бейєра, який використовується для диференціації алкенів від ізомерних цикланів.
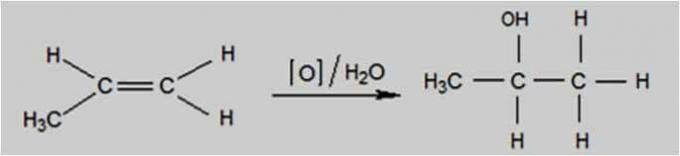
Реакція легкого окислення
Окислення енергії
При цьому типі окислення перманганат калію знаходиться в більш гарячому та кислому середовищі, що робить реакцію більш енергійною. Енергійні окислювачі можуть розірвати подвійний зв’язок алкенів.
Залежно від структури алкену можуть утворюватися кетони та карбонові кислоти.
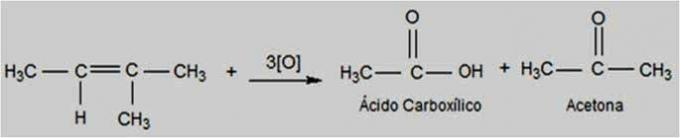
Реакція окислення енергії
Хочете знати більше? Також читайте про Електрохімія.