О атомний промінь елементів - це періодична властивість, що визначає радіус атома, який змінюється залежно від положення елемента в Періодичній системі.
Таким чином, вони можуть збільшуватися і зменшуватись як атомний номер (Z) елемента, що відповідає кількості протонів, присутніх в ядрі атомів.
Підводячи підсумок, атомний радіус відповідає половині відстані між ядрами двох сусідніх атомів, виражаючись таким чином:
r = d / 2
звідки:
р = радіус
d = міжядерна відстань
Як правило, атомний радіус вимірюється в пікометрах (pm), кратному лічильнику (1 пікометр = 10-12 м.). Зверніть увагу, що коли посиланням є не атом, а іон, знайденим радіусом є іонний радіус.
Варіація атомного радіуса
У таблиці Менделєєва зростання атомного радіуса можна побачити на наступному малюнку:
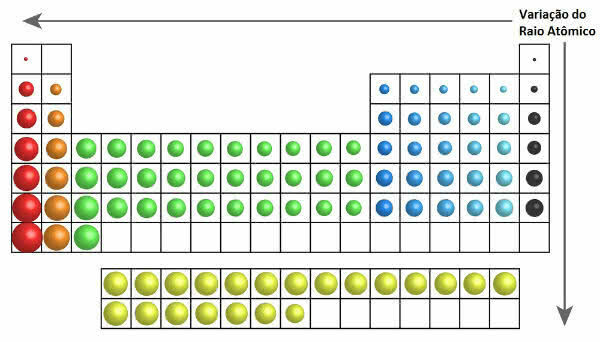 Зміни атомного радіуса в періодичній системі
Зміни атомного радіуса в періодичній системі
Таким чином, по вертикалі (сімейства або групи) атомний радіус збільшується зверху вниз. По горизонталі (крапки) вони збільшуються справа наліво.
Дивіться зворотну варіацію в Електронна спорідненість і електронегативність.
Енергія іонізації
THE енергія іонізації (або потенційна) це також періодична властивість, що визначає енергію, необхідну для зсуву електрона, що виражається в електрон-вольтах (еВ).
Читайте також: Періодичні властивості.
Перевірте запитання на вступному іспиті з коментованою резолюцією у: Вправи на Періодичній системі.