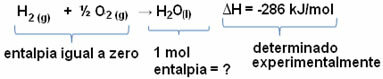
Каталізатори - це речовини, здатні прискорити реакцію без змін, тобто вони не витрачаються під час реакції.
Щоб зрозуміти, як працюють каталізатори, нам потрібно пам’ятати, що було пояснено в тексті "Енергія активації”. Як показано там, для початку хімічної реакції необхідно, щоб реагенти мали або отримували певну кількість мінімальної енергії, яка називається енергія активації.
При цій мінімальній енергії реагенти можуть досягати активований комплекс, який є проміжним станом (перехідним станом), що утворюється між реагентами та продуктами, в якому У структурі існують ослаблені попередні ланки та утворення нових ланок (наявних у продукції).
Наприклад, розглянемо загальну реакцію нижче:
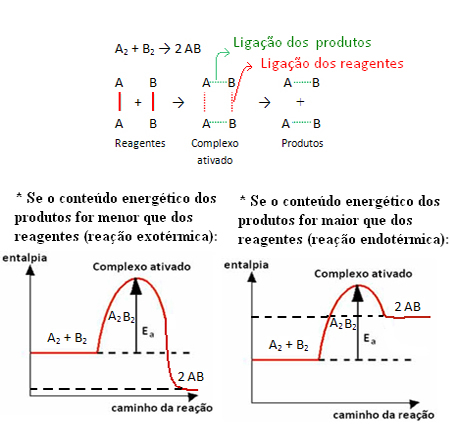
Зверніть увагу, що енергія активації, необхідна для досягнення активованого комплексу, стає свого роду перешкодою, яку потрібно подолати, щоб відбулася реакція. Це означає, що чим більша енергія активації реакції, тим більша перешкода повинна бути подолана і повільніша швидкість реакції.
Вірно і протилежне, якщо енергія активації нижча, реакція буде швидшою. це саме те
каталізатори вони вони створюють альтернативний шлях, який вимагає менше енергії активації, завдяки чому реакція протікає швидше.Не зупиняйтесь зараз... Після реклами є ще щось;)

Для того, щоб знизити енергію активації, каталізатор діє, змінюючи механізм реакції, комбінуючись з реагентами в системі, яка може бути однофазною (гомогенний каталіз) або багатофазною (гетерогенний каталіз).
Детальніше про ці типи каталізу можна побачити в текстах нижче:
- однорідний каталіз
- гетерогенний каталіз
Але, загалом кажучи, можна сказати, що це Поєднання реагенту та каталізатора утворює проміжне з'єднання, яке потім трансформується, утворюючи продукт і каталізатор. Зверніть увагу, як це можна представити:
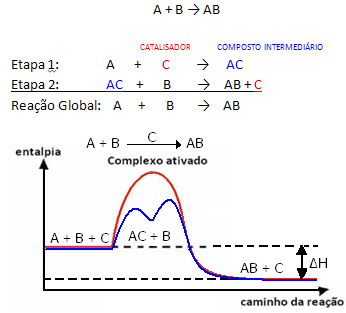
Переконайтеся, що каталізатор відновлюється в кінці реакції, не витрачаючись ним.
Важливим фактом є це каталізатор прискорює як пряму, так і зворотну реакції, це означає, що це зменшує енергію активації обох.
Дженніфер Фогача
Закінчив хімію
Чи хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. «Як діють каталітичні речовини?»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/como-atuam-as-substancias-catalisadoras.htm. Доступ 27 червня 2021 року.