Розглянемо дві батареї, що оточують мідний електрод:

Цинково-мідні та мідно-срібні батареї.
У першій комірці, відомій як клітина Даніелла, електроди зроблені з цинку та міді, і ми помічаємо, що цинк зазнає окислення, тобто він віддає електрони міді, будучи, таким чином, анодом. Мідний електрод, у свою чергу, працює як катод, приймаючи електрони і відновлюючись.
Однак можна помітити, що у другій купі, мідно-срібних електродах, мідь працює не як катод, а як анод, окислюючись цього разу.
Це показує нам, що порівнюючи ці три електроди, тенденція до зменшення працює наступним чином:
| Цинк |
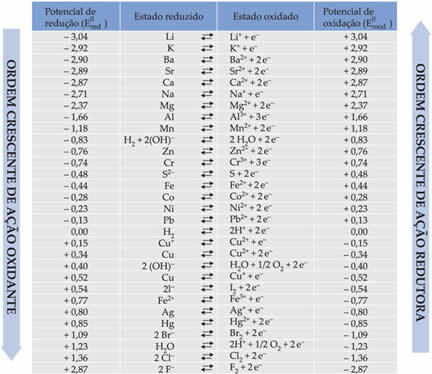
Таким чином, ця здатність зазнавати зменшення називається Потенціал зменшення (Eчервоний). Оскільки це значення залежить від тиску, температури та концентрації розчину, a стандартний потенціал (або нормальний, при 25 ° C, тиск 1 атм і концентрація 1,0 моль / л), який позначається символом І0. Вірно і навпаки, існує Потенціал окислення (Eокси), який у цьому випадку має зростаючий порядок:
| Цинк> Мідь> Срібло |
Чим нижчий стандартний потенціал відновлення, тим більша здатність металу віддавати електрони і навпаки. Так само, чим нижчий стандартний потенціал окислення, тим більша здатність металу приймати електрони і навпаки.
| У купі вид з найвищим Ered зазнає редукції, а інші види з найвищим Eoxy окислюються. |
Якщо ми адаптуємо вольтметр, як на малюнку вище, до однієї з цих комірок, буде вимірюватися інтенсивність електричного струму, що виробляється ними, тобто його електрорушійна сила (ЕРС або Е) або різниця потенціалів (U або ddp) *. Значення вказано у вольтах (V), що зазвичай відображається на акумуляторних батареях та етикетках.
Не зупиняйтесь зараз... Після реклами є ще щось;)

Різниця потенціалів (U або ddp) батареї, показана на етикетці.
Електрорушійна сила може бути виражена через відновлення або потенціал окислення. Важливо пам’ятати про це ці потенціали мають однакове значення, але мають протилежні знаки.
Для розрахунку напруги акумулятора в стандартному стані ми використовуємо такий вираз:
| ∆І0 = І0червоний (катод) - І0червоний (анод) |
або
| ∆І0 = І0окси (анод) - І0окси (катод) |
Таким чином, абсолютні значення кожного електрода відображаються не на вольтметрі, а різниці потенціалів між ними.
* Ми вважаємо різницю потенціалів рівною електрорушійній силі, оскільки розрахунок різниці потенціалів генератора дається рівнянням: U = E - r.i, де:
U = різниця потенціалів
E = електрорушійна сила
r = внутрішній опір
i = інтенсивність електричного струму
Але в хімії ми розглядаємо батареї як ідеальні генератори, так що їх внутрішній опір є незначним стосовно електричного кола. Отже, маємо, що U = E.
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. "Різниця потенціалів акумулятора"; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/diferenca-potencial-uma-pilha.htm. Доступ 28 червня 2021 року.