Карбонати - це неорганічні сполуки, утворені іонним зв’язком металу або напівметалу з карбонатним аніоном, CO32-.
Вуглець чотиривалентний, тобто він має чотири електрони у валентній оболонці, і він може зробити чотири ковалентні зв’язки стабільними, в той час як кисень є двовалентним, маючи шість електронів у валентній оболонці і будуючи два зв’язки, щоб бути стабільним, з вісьмома електрони. Таким чином, існує сильна тенденція вуглецю зв’язуватися з двома атомами кисню, які є стабільними (O ═ C ═ O → CO2).
Але інший кисень може поєднуватися з вуглецем, оскільки співвідношення іонних радіусів призводить до координаційного числа, рівного 3, утворюючи структуру трикутний, в якому вуглець знаходиться в центрі, утворюючи подвійний зв’язок з одним з атомів кисню і два одинарних зв’язки з двома іншими кисню. Результатом є два надлишкових електрони, оскільки ці два кисню не є стабільними, і потрібно отримувати по одному електрону кожен:
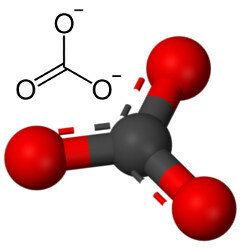
Карбонатний аніон утворюється ковалентними зв’язками, але його сполуками, які є неорганічними солями та мінералами відомі як карбонати, є іонними, оскільки цей радикал отримує два електрони від якогось металу або напівметалу, утворюючи а іонний зв’язок.
Ці сполуки не розчиняються у воді, за винятком карбонату амонію ((NH4)2CO3) та карбонати, утворені лужними металами (елементи сімейства 1: Li, Na, K, Rb, Cs та Fr). Майже всі це білі тверді речовини, як показано на зображенні нижче:

Два найпоширеніші та найважливіші повсякденні приклади карбонатів - це карбонат натрію (Na2CO3) і карбонат кальцію (CaCO3). У першому випадку натрій належить до сімейства 1, що має електрон у валентній оболонці і прагне втратити цей електрон, щоб стати стабільним. Оскільки карбонатний аніон повинен отримати два електрони, він зв'язується з двома атомами натрію:
Не зупиняйтесь зараз... Після реклами є ще щось;)

Сода кальцинована більше відома як сода або сода, використовується у виробництві мила, барвників, ліків, паперів та для лікування води в басейні. Але основним його застосуванням є карбонат кальцію та пісок у виробництві скла.
Кальцій - це родина 2, яка має тенденцію втрачати два електрони. Таким чином, атом кальцію зв'язується з карбонатним радикалом:

Карбонат кальцію присутній у вапняку та мармурі. В сталактити та сталагміти що існують у печерах, складаються з цього карбонату; черепашки, коралові рифи та яєчна шкаралупа теж. Побіляючи стіни, стовбури дерев та інші місця, ми використовуємо гідроксид кальцію (Ca (OH)2), який з часом реагує з атмосферним вуглекислим газом, утворюючи карбонат кальцію.

Карбонати дуже поширені на поверхні Землі, як і у випадку з мінералами. Їх кристалічні решітки можуть переставляти себе в просторі двома способами: орторомбічним (як у випадку з мінералом арагонітом, показаним вище разом із формулою карбонату кальцію) та ромбоедричний або тригональний, як у випадку кальциту (іншого мінералу, що складається з карбонату кальцію).
Карбонати реагують у присутності кислот, виділяючи СО2, що легко помітити через шипучість.
Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. «Карбонати»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/carbonatos.htm. Доступ 28 червня 2021 року.
Хімія

Карбонат натрію, метод Леблана, метод Ернеста Солвея, кальцинована сода, сода, виробництво звичайного скла, обробка води в басейні, контроль рН води, обробка текстилю, харчова добавка.
Хімія

Щоденні солі, карбонат кальцію, хлорид натрію, фторид натрію, нітрат калію, нітрат натрію натрій, карбонат натрію, бікарбонат натрію, бікарбонат натрію, сульфіт натрію, селітра, сода.

