У тексті "Заголовок або масовий відсоток”Ми побачили, як розрахувати співвідношення між масою розчиненої речовини та масою розчину для твердих, рідких та газоподібних розчинів. Однак у цьому тексті ми побачимо, що можна також розрахувати титр за об’ємом для розчинів з рідкими або газоподібними компонентами.

Заголовок за обсягом можна обчислити виразом:
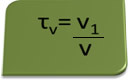
Розглянемо як приклад водний розчин етилового спирту, що використовується як антисептик і дезінфікуючий засіб, який був готується шляхом додавання 70 мл чистого спирту до такої кількості води, щоб довести об'єм 100 мл рішення. Отже, маємо:
τ = 70 мл = 0,7
100мл
Ми також можемо виразити заголовок у відсотках, просто помноживши результат на 100%. Отже, у цьому випадку ми маємо 70% розчин етилового спирту, це означає, що із кожних 100 об’ємних одиниць розчину 70 об’ємних одиниць - це спирт.
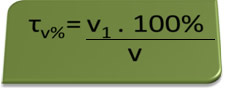
У наведеному нижче випадку ми маємо 70% розчин етилового спирту в обсязі 250 мл розчину; що означає, що 175 мл - це спирт, згідно з розрахунками:
100 мл 70 мл спирту
250 мл х
x = 70. 250
100
Х = 175 мл алкоголю

Однак ми не можемо сказати, що в цьому випадку ми маємо 75 мл (250-175) води. На відміну від масового титру, в якому ми можемо додати масу розчинника до маси розчиненої речовини, щоб знайти масу розчину, цього не можна зробити щодо об'ємного титру.

Не зупиняйтесь зараз... Після реклами є ще щось;)
Це означає, що об’єм розчину не дорівнює сумі об’єму розчинника та об’єму розчиненої речовини (хоча часто різницю можна вважати незначною). Це пов’язано з тим, що міжмолекулярні сили, що існують у цих рідинах, впливають на кінцевий об’єм.
У випадку з вищезазначеним розчином етилового спирту, наприклад, коли ми змішуємо спирт з водою, відбувається скорочення загального обсягу розчину; тобто кінцевий об’єм буде меншим, ніж якщо б ми додали об’єм алкоголю та води. Це пов’язано з тим, що молекули алкоголю встановлюють зв’язки або водневі зв’язки з молекулами води, зменшуючи простір між ними.
Отже, в цьому та інших випадках об’єм розчину слід вимірювати експериментально, коли це не передбачено у вправі.
Процентний відсоток широко використовується у випадках з алкогольними напоями та комерційним алкоголем, як зазначалося вище. Дивіться два важливі програми цього розрахунку:
- Алкотестер: алкотестер вимірює концентрацію етилового спирту в крові, і в Бразилії заборонено їздити на будь-якому транспортному засобі із вмістом алкоголю в крові рівним або перевищує 0,1% за обсягом. Людина з таким вмістом алкоголю має на кожен літр крові 1 мл алкоголю, як показують такі розрахунки:
τv%=V1. 100%
v
0,1 % = V1. 100%
1л
V1 = 0,1% → V1 = 0,001 л = 1 мл
100%

- Вміст етанолу в бензині: у Бразилії бензин регулюється додаванням етанолу. Але вміст етанолу в бензині повинен становити не більше 24 об.% Безводного спирту (оскільки бензин повинен бути безводним). Чим більше етанолу додається до бензину, тим більше колір палива стає світлішим і збільшується його щільність.
Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. "Назва обсягу хімічного розчину"; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/titulo-volume-uma-solucao-quimica.htm. Доступ 28 червня 2021 року.
Хімія

Як працює алкотестер, концентрація алкоголю, алкотестер, реакції з етиловим спиртом, типи алкотестери, дихромат калію, паливний елемент, каталізатор, вивільнення електронів, оцтова кислота, водень, концепт
