О обчислення кількості атомних частинок використовується для позначення кількості протонів (в ядрі), електронів (в електросфері) та нейтронів (в ядрі), присутніх у будь-якому атомі чи іоні. Для цього важливо знати деякі характеристики атомів:
1- Атомний номер (Z)
Це математичний код, представлений великою літерою Z, розташований у нижній лівій частині абревіатури атома:
ZX
Він вказує кількість протонів (p) в ядрі та кількість електронів (e) в електросфері атома. Отже, загалом:
Z = p = e
2- Масове число (A)
Це математичний код, який відповідає сумі кількості протонів (p) і нейтронів (n), присутніх в ядрі будь-якого атома. Рівняння, яке представляє масове число, дається формулою:
A = p + n
Оскільки кількість протонів дорівнює атомному номеру, ми можемо написати рівняння для обчислення масового числа таким чином:
A = Z + n
Якщо ми знаємо масове число та атомний номер атома, ми можемо визначити кількість нейтронів наступним чином:
n = A - Z
3- іони
Вони є атомами, які втрачають або отримують електрони. Вони мають позитивний або негативний знак, розташований у правому верхньому куті їх зображення, як у такій моделі:
X+ або X-
Позитивний іон: Це називається катіоном, а позитивний знак вказує на те, що він втратив електрони.
Негативний іон: це називається аніоном, а негативний знак вказує на те, що він набрав електрони.
Не зупиняйтесь зараз... Після реклами є ще щось;)
4- Атомна подібність
а) Ізотопи
Атоми, що мають однаковий атомний номер та різні масові числа. Приклад:
7X14 і 7Y16
Атоми X і Y мають однаковий атомний номер (ліворуч від абревіатури), тобто дорівнює 7. Атом X має масове число (праворуч від абревіатури), що дорівнює 14, а атом Y має масове число, рівне 16.
б) Ізобари
Атоми, що мають однакове масове число та різні атомні числа. Приклад:
15X31 і 13Y31
Атоми X і Y мають масове число (праворуч від абревіатури), яке дорівнює 31. Атом X, навпаки, має атомне число, рівне 15, а атом Y має атомне число, рівне 13.
в) Ізотони
Атоми, що мають різні масові числа та атомні номери, але однакову кількість нейтронів.
г) Ізоелектроніка
Атоми, що мають однакову кількість електронів. Приклад:
12X+2 і 7Y-3
Атом X має атомне число, рівне 12, і є катіоном (з позитивним зарядом +2), тому він втрачає два електрони, маючи таким чином 10 електронів у своїй електросфері. Атом Y, навпаки, має атомне число, рівне 7, і є аніоном (з негативним зарядом -3), тому він отримує три електрони, маючи таким чином 10 електронів у своїй електросфері.
Карта розуму: атомні частинки
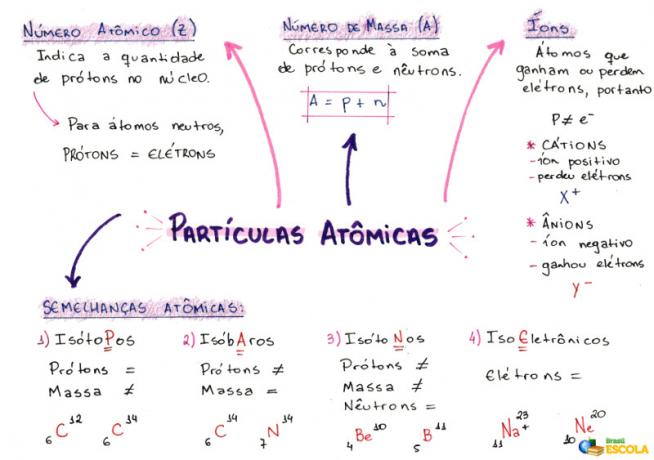
* Щоб завантажити карту розуму в PDF, Натисніть тут!
Приклади розрахунку кількості атомних частинок
Приклад 1: Визначте кількість протонів, нейтронів та електронів в атомі 14X29.
Були наведені наступні значення для атома X:
Масове число (вгорі праворуч) = 29
Атомне число (зліва внизу) = 14
Для визначення кількості протонів:
Кількість протонів завжди дорівнює атомному номеру, тому атом Х має 14 протонів.
Для визначення кількості електронів:
Оскільки атом X не є іоном, тому кількість електронів дорівнює кількості протонів, тобто 14.
Для визначення кількості нейтронів:
Кількість нейтронів визначається з використанням кількості маси та протонів у такій формулі:
A = p + n
29 = 14 + п
29 - 14 = п
n = 15
Приклад 2: Визначте кількість протонів, нейтронів та електронів іона X+3, знаючи, що їх масове число та атомний номер складають відповідно 51 та 23.
Були наведені наступні значення для іона X:
Масове число = 51
Атомне число (зліва внизу) = 23
Для визначення кількості протонів:
Кількість протонів завжди дорівнює атомному номеру, тому атом Х має 23 протони.
Для визначення кількості електронів:
Іон X позитивний (+3), отже, це катіон, який втратив три електрони. Отже, кількість його електронів дорівнює 20.
ПРИМІТКА: Зменшення або збільшення числа електронів завжди відбувається відносно атомного числа.
Для визначення кількості нейтронів:
Кількість нейтронів визначається з використанням кількості маси та протонів у такій формулі:
A = p + n
51 = 23 + п
51 - 23 = п
n = 28
Приклад 3: Атом W має атомний номер і масу, рівні 29 і 57 відповідно, будучи ізобаром a атом Y, який має атомне число, що дорівнює 30, що є ізотопом атома B, масове число якого дорівнює 65. За цією інформацією визначте кількість протонів, нейтронів та електронів в атомі В.
Дані, надані вправою:
Атом W
атомний номер (зліва внизу) = 29
масове число (вгорі праворуч) = 57
Y ізобара, тобто маса Y також дорівнює 57.
Атом Y
атомний номер = 30
масове число = 57
За цими двома значеннями ми повинні визначити його нейтронне число, оскільки це ізотон елемента В:
A = Z + n
57 = 30 + п
57 - 30 = п
n = 27
Атом В:
масове число = 65
число нейтронів = 27
За цими даними ми повинні визначити його атомний номер, тому що за допомогою цього ми будемо визначати його кількість протонів та кількість електронів (оскільки це не іон):
A = Z + n
65 = Z +27
65 - 27 = Z
Z = 38
Отже, атом В має 38 протонів, 38 електронів і 27 нейтронів.
* Карта розуму Віктора Рікардо Феррейри
Вчитель хімії
Мені Діого Лопес Діас