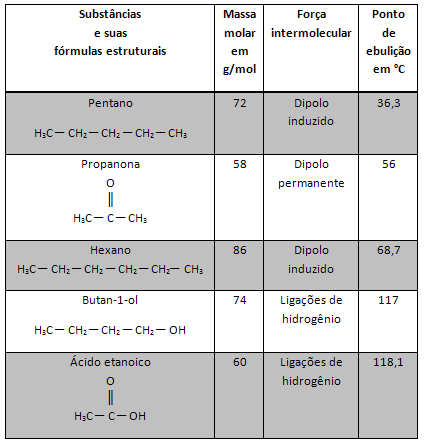
Реакції окиснення-відновлення, що вивчаються в основному з фізичної хімії, - це ті, в яких відбувається перенос електронів. Реагуючий вид (атом, іон або молекула), який втрачає один або кілька електронів, є тим, що зазнає окислення. З іншого боку, хімічний вид, який отримує електрони, зменшується.
Як правило, коли цей тип реакції вивчається в неорганічній хімії, він називається проста реакція обміну або переміщення.
Щоб будь-яка реакція відбулася, необхідно задовольнити певні умови. Один з них - це те, що має бути хімічна спорідненість між реагентами, тобто вони повинні взаємодіяти таким чином, щоб забезпечити утворення нових речовин.
У разі окислювально-відновних реакцій спорідненість означає, що один з реагентів прагне набирати електрони, а інший - втрачати електрони. Ця тенденція відповідає реактивність залучених хімічних елементів.
Подивимось, як можна порівняти реакційну здатність між металами.
Припустимо, що ми хочемо зберігати розчин мідного сульфату II (CuSO4). Ми не могли помістити цей розчин в алюмінієву ємність, оскільки могла відбутися така реакція:
2 Ал(s) + 3 CuSO4 (вод.)→ 3 Cu(s) + Ал2(ТІЛЬКИ4)3 (вод.)
Зверніть увагу, що алюміній окислюється, втрачаючи по 3 електрони кожен і стаючи катіоном алюмінію:
Ал(s) → Ал3+(тут) + 3 і-
Одночасно катіон міді (Cu2+), який був у розчині, отримував електрони з алюмінію і відновлювався, стаючи металевою міддю. Кожен катіон міді отримує два електрони:
Дупу2+(тут) + 2 і- → Cu(s)
Однак, якби було навпаки, і ми хотіли зберігати розчин сульфату алюмінію (Al2(ТІЛЬКИ4)3 (вод.)), не буде проблемою покласти його в мідний контейнер, оскільки така реакція не відбудеться:
Дупу(s) + Ал2(ТІЛЬКИ4)3 (вод.) → не відбувається
Ці спостережувані факти можна пояснити тим, що алюміній є більш реакційноздатним, ніж мідь.
Метали мають тенденцію віддавати електрони, тобто окислюватися. Порівнюючи різні метали, той, що має найбільшу тенденцію віддавати електрони, є найбільш реактивним. Отже, реакційна здатність металів також пов'язана з їхньою енергія іонізації, тобто мінімальна енергія, необхідна для видалення електрона з газоподібного атома в основному стані.
Не зупиняйтесь зараз... Після реклами є ще щось;)

Виходячи з цього, черга реактивності металу або ряд електролітичних напруг, показано нижче:
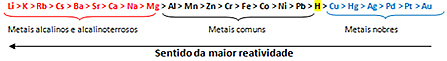
Найреактивніший метал реагує з іонними речовинами, катіони яких є менш реактивними. Іншими словами, метал зліва реагує з речовиною, утвореною іонами праворуч. Навпаки не буває.
Згадавши наведений приклад, у рядку реакційної здатності подивіться, що алюміній (Al) знаходиться ліворуч від міді (Cu). Тому алюміній реагує з розчином, утвореним катіонами міді; але мідь не реагує з розчином, утвореним катіонами алюмінію.
Зверніть увагу, що найбільш реактивним металом є літій (Li), а найменш реакційноздатним є золото (Au).

Це одна з причин, чому золото настільки цінне, тому що, якщо воно не реагує, воно залишається цілим надовго. Це видно з позолочених єгипетських саркофагів та скульптур, що датуються найдавнішою античністю. Ми також візуалізуємо це, порівнюючи довговічність ювелірних виробів із чистого золота та ювелірних виробів з інших металів, які є більш реактивними, ніж золото.

Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. «Порядок реактивності металів»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/ordem-reatividade-dos-metais.htm. Доступ 28 червня 2021 року.