İyonizasyon, suya yerleştirilen moleküler maddelerden iyonları oluşturan kimyasal bir reaksiyondur.
O halde iyonlaşma diyebiliriz süreciiyon oluşumu.
Asitler, suya konulduğunda iyonlaşmaya uğrayan maddelere örnektir.
iyonlaşma süreci
Aşağıdaki örnekte iyonlaşma sürecinin nasıl gerçekleştiğini görün:
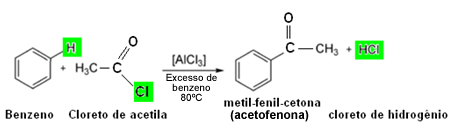
Suya konulduğunda hidroklorik asit (HCl) iyonizasyona uğrar. H ve Cl arasındaki kimyasal bağ kırılır ve H iyonları oluşur.+ ve Cl-, su ile çevrili olan.
Gördüğümüz gibi, H+ bir elektron ve Cl kaybetti- bir elektron aldı. Bununla birlikte, H+ stabilize olması gerekir ve bu nedenle suya bağlanır.
Böylece, HCl iyonizasyon reaksiyonu aşağıdaki gibi de temsil edilebilir:
Şimdi hidronyum katyonunun oluşumunu gözlemliyoruz (H3Ö+), H'nin birleşmesinin sonucu+ ve H'den2Ö.
Bu örnekte Cl'nin elektronu aldığına dikkat etmek de önemlidir, çünkü en çok odur. elektronegatifyani elektron kazanma eğilimi vardır. Bu nedenle elektronları kolayca kendine çekerdi.
Siz de okuyun:
- elektronlar
- iyon, katyon ve anyon
- Kimyasal reaksiyon
Diğer iyonizasyon örneklerine göz atın:
1)
2)
bu iyonlaşma enerjisi veya iyonlaşma potansiyeli, temel durumdaki bir atomdan bir elektronu aktarmak için gereken enerji miktarını gösteren periyodik bir özelliktir.
Ayrışma ve İyonizasyon
bu ayrışma kimyasal bir tepkime değil, fiziksel bir olaydır. Sudaki iyonik bileşiklerden mevcut iyonların salınmasını ifade eder.
Ayrışma ve iyonlaşma arasındaki temel fark:
- İyonizasyon: iyonlar oluşur;
- Ayrışma: mevcut iyonların ayrılması.
Ayrışma işlemi sadece tuzlar ve bazlar ile gerçekleşir. Örnek: NaCl, sofra tuzu.
Serbest iyonlar moleküllerden daha reaktif olduğundan, ayrışma ve iyonlaşma kimyasal reaksiyonların gerçekleşmesi için önemli süreçlerdir.
Siz de okuyun:
- asitler
- tuzlar
- bazlar
- iyon dengesi
- pH ve pOH kavramı ve belirlenmesi
- Nötrleştirme reaksiyonu
Konuyla ilgili giriş sınavı sorularını yorumlanmış bir çözümle birlikte kontrol ettiğinizden emin olun: inorganik fonksiyonlarla ilgili alıştırmalar.