Bu metinde nasıl bir tablosu fiziksel durum değişikliği herhangi birine saf madde, bu tür diyagramların nasıl yorumlanacağı ve karışımların grafiğinin nasıl temsil edildiği.
Bunun için su örneğini ele alalım. –10 ºC sıcaklıktaki bir bardak buzu alıp 1 atm basınçta ısıtma işlemine başladığımızı düşünün. Sıcaklık arttıkça, -10 ºC'den -9 ºC'ye, -8ºC'ye vb. gidildikçe, buz 0 ºC sıcaklığa ulaşana kadar katı halde kalacaktır.
Bu noktada sıvı hale geçmeye yani füzyon gerçekleşmeye başlar. Sıcaklık daha önce olduğu gibi artmaya devam etmeyecek, ancak tüm buz eriyene kadar 0°C'de sabit kalacaktır:

Tüm katıyı erittikten sonra, sistemin sıcaklığı 100°C sıcaklığa ulaşana kadar artmaya devam edecektir. Bu sıcaklıkta sıvı halde bulunan su buhar haline geçmeye başlayacak yani kaynayacaktır.
Tıpkı olayda olduğu gibi füzyon noktası, kaynama noktasında, sıcaklık da tüm sıvı buharlaşana kadar sabit kalacaktır. Bundan sonra sistemi ısıtmaya devam edersek sıcaklık yükselmeye devam edecek:
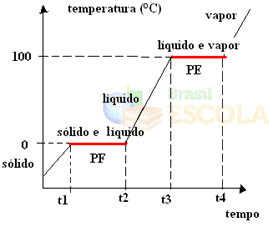
Hazır! Bu, suyun fiziksel durumundaki veya ısınma eğrisindeki değişimi temsil eden grafik veya diyagramdır. Ters süreç olsaydı, aşağıdaki su soğutma eğrisine sahip olurduk:
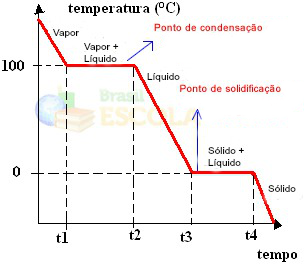
Bu grafiklerin çok önemli bir yönü, iki seviyeden oluşmasıdır, yani sıcaklığın bir süre sabit kaldığı iki nokta vardır. Bu her zaman saf bir maddenin hal değişiminde meydana gelir. Tek fark erime ve kaynama noktası değerleridir.
Örneğin oksijen, sudan farklı olarak sıvı değil, oda sıcaklığında (yaklaşık 20ºC) bir gazdır. Bunun nedeni, deniz seviyesinde erime noktasının -223.0 °C ve kaynama noktasının -183.0 °C olmasıdır. Fiziksel durum değişim grafiğinize bakın:

Ortak karışım grafikleri
Bir karışımı ısıtıyor veya soğutuyorsak, erime noktası ve kaynama noktası değişmez. belirlenmiş ve sabit değerler, yani grafiklerde gözlenen iki seviye oluşmayacaktır. yukarıda.
Fiziksel durumlardaki değişiklikler, sabit bir miktar yerine sıcaklık aralıklarında meydana gelecektir. Örneğin erime noktası belirli bir sıcaklıkta başlayacak ve başka bir sıcaklıkta sona erecek ve aşağıdaki grafikte gösterildiği gibi kaynama noktasında da aynı şey gerçekleşecek:
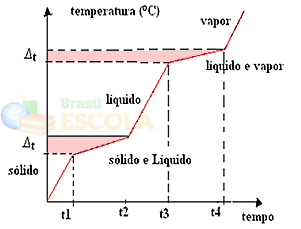
İki istisna ötektik ve azeotropik karışımlardır. Onlara ne olduğunu görün:
a) Ötektik karışım
Ötektik karışım, füzyon sırasında saf bir maddeymiş gibi davranır, yani bu noktada sıcaklık, agregasyon hal değişiminin başlangıcından sonuna kadar sabit kalır.

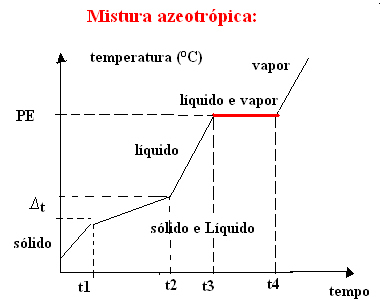
b) azeotropik karışım
Azeotropik karışım kaynama sırasında saf bir madde gibi davranır, yani bu noktada agregasyon durumundaki değişimin başlangıcından sonuna kadar sıcaklık sabit kalır.
Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/graficos-mudanca-estado-fisico.htm
