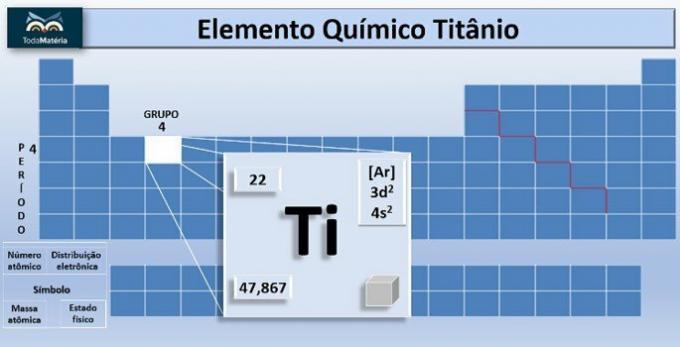
Ö titanyum sembolü Ti olan ve atom numarası yani proton sayısı 22'ye eşit olan kimyasal elementtir. Bu metal periyodik tablonun 4. ve 4. grubunda yer alır.
Elementin atom kütlesi 47.867 u'dur ve atomun elektronlarında 22 elektron bulunduğundan elektron dağılımı 1s'dir.2 2s2 2p6 3s2 3p6 4s2 3 boyutlu2.
Titanyum, çelik kadar güçlü ve çok daha hafif olduğu için sayısız uygulama için arzu edilen özelliklere sahiptir.
Sünek, refrakter, korozyona dayanıklı bir metal olduğu için mekanik dayanım gösterir, termal kararlılık ve düşük reaktivite, metal alaşımlarına eklenir, böylece yüksek verim. Biyouyumluluğu ve toksik olmaması, kemik protezlerinin yapımında da faydalı olmasını sağlar.
Titanyumun ana özellikleri şunlardır:
- Erime noktası: 1668 °C
- Kaynama noktası: 3287 °C
- Yoğunluk: 4,5 g/cm3
- Renk: gümüş grisi
- 20 °C'de fiziksel durum: katı
- İzotoplar: Ti46, sen47, sen48, sen49 ve sen50
Bu kimyasal element 1791 yılında İngiliz William Gregor tarafından keşfedilmiştir ve adı Yunancadan türetilmiştir. devler, daha sonra Martin Heinrich Klaproth tarafından atfedildi.
Titanyum gezegende en bol bulunan dokuzuncu elementtir ve yerkabuğunda rutil (TiO) gibi cevherlerde bulunur.2) ve ilmenit (FeTiO3). Bu nedenle madencilik, bu metali elde etmenin ana yöntemidir.
Titanyum ne için kullanılır?
Oda sıcaklığında kimyasal olarak reaksiyona girmemesi, kolay kalıplanması, mekanik ve korozyon direncinin yüksek olması nedeniyle titanyum stratejik bir metal olarak kullanılır.
Havacılık ve uzay endüstrileri, türbin ve gövde bileşenleri gibi parçaların üretimi için titanyumun ana kullanıcılarıdır. Diğer uygulamalar diş protezleri, cerrahi implantlar ve mücevher imalatıdır.
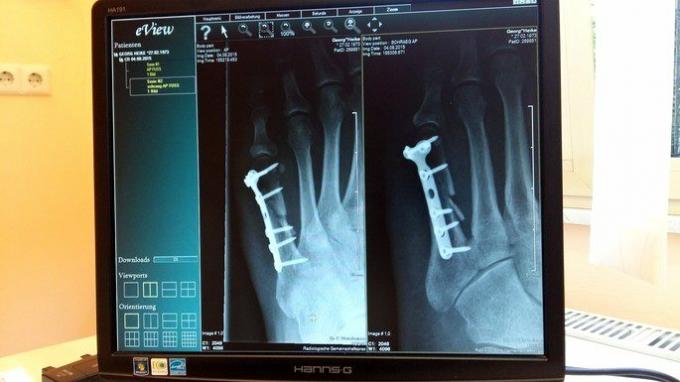
Tıpta titanyum, insan dokularıyla uyumluluğu, hafifliği ve sağlamlığı nedeniyle çok faydalıdır. Diğerlerinin yanı sıra sabitleme vidaları, diz eklemi değiştirme, humerus protezi, kalça protezi gibi vücut parçalarına yönelik implantların üretiminde kullanılır.
Titanyum dioksit (TiO2) ağartma maddesi olarak kullanılan bu elementin ana bileşiklerinden biridir. Genel olarak, yüksek kaliteli beyaz mürekkepler, rengin ve parlaklığın görsel görünümünü iyileştirmek için kullanır. Diş macunları ve güneş kremleri gibi diğer ürünler de pigmenti kullanır. Süt ürünlerine, tatlılara ve içeceklere eklenen gıda boyası olarak da uygulaması vardır.
Mimaride, kuzey İspanya'daki Bilbao'daki Guggenheim Müzesi'nde kavisli yapıları kaplamak için titanyum kullanımını görebiliriz.

Günlük yaşamda bisiklet çerçeveleri, gözlükler ve tenis raketleri gibi bileşiminde titanyum bulunan sayısız ürün bulabiliriz.
Kimya endüstrisinde titanyum, reaksiyonlar için bir katalizör olarak kullanılır. Bu şekilde, maddelerin bileşimini etkilemeden reaksiyon hızının kontrol edilmesini ve ürün oluşum süresinin azaltılmasını mümkün kılar.
Otomobil endüstrisi, kütlelerini azaltmak ve böylece yakıt tüketimini azaltmak ve hızlanmalarını artırmak için otomobillerin imalatına titanyumun dahil edilmesini araştırdı.
İçerikle daha fazla bilgi edinin:
- Kimyasal elementler
- Periyodik tablo
- Metaller nelerdir?
Bibliyografik referanslar
ATKİNS, P.W.; JONES, L. Kimyanın ilkeleri: modern yaşamı ve çevreyi sorgulamak. 3.ed. Porto Alegre: Bookman, 2006.
FELT, R. Kimyanın Temelleri: cilt. bekar. 4. baskı. Sao Paulo: Moderna, 2005.
Lee, J. D. O kadar da özlü inorganik kimya değil. 5. baskının çevirisi. İngilizce. Yayıncı Edgard Blucher Ltd. 1999.