Hidronyum iyonlarının (H) mol/L cinsinden aynı konsantrasyonuna sahip olan bir ortam nötr olarak kabul edilir.3Ö+) ve hidroksit (OH-).
Diğer çözeltiler için standart bile olan bir nötr ortam örneği, 25ºC sıcaklıkta saf, damıtılmış sudur. Bu sıcaklıkta tam olarak 1. 10-7 her iki iyonun mol/L'si. Bu nedenle, iyonik ürününüz (Kw) 10'a eşittir-14 (mol/L)2:
Kw = [H3Ö+]. [Ah-]
Kw = (1. 10-7 mol/L). (1. 10-7 mol/L) = 10-14 (mol/L)2
pH ve pOH aşağıda verilmiştir:
pH= - günlük [H3Ö+] pOH= -log[OH-]
pH= - günlük 1. 10-7 pOH= - günlük 1. 10-7
pH = 7pOH = 7
Bu bize gösteriyor ki, nötr bir çözümde, pH, pOH'ye eşittir.
- Asit ortamı:
Asidik bir ortamda, H iyonlarının konsantrasyonu3Ö+ OH iyonlarından daha büyüktür-.
Böyle bir çözüm, H iyonlarının küçük bir kısmı eklenerek elde edilebilir.3Ö+örneğin, bir asit vasıtasıyla.
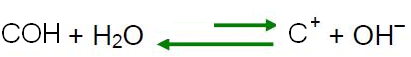
Le Chatelier ilkesine göre, dengedeki bir sistemde bir bozulmaya neden olduğunda, bu kuvvetin etkilerini azaltmak için kendini yeniden ayarlama eğilimindedir. Bu, suya bir asit eklenirse, H iyonlarının
3Ö+ fazla olacaklar ve denge ters reaksiyon yönünde sola kayacak. Böylece bu fazla iyonlar OH iyonları ile reaksiyona girecek-. Böylece, OH iyonlarının konsantrasyonu- azalacak ve çözelti asidik hale gelecektir.
İyonik ürün (Kw) her zaman 10'a eşittir-14, ancak H iyonlarının konsantrasyonu3Ö+ OH iyonlarının konsantrasyonundan daha büyüktür-1. Bu nedenle, asidik bir ortamda pH, pOH'den daha büyüktür, ancak toplamı her zaman 14'e eşittir.
Ayrıca, H iyonlarının konsantrasyonu arttıkça3Ö+, pH değeri o kadar büyük olur. Oda sıcaklığında (25°C), pH < 7 ve pOH > 7.

- Temel araçlar:
Bazik ortamda, OH iyonlarının konsantrasyonu- H iyonlarından daha büyüktür3Ö+.
Suya baz eklersek, OH iyonları ekliyoruz demektir.- ve bir önceki maddede açıklandığı gibi, Le Chatelier ilkesiyle, reaksiyonun dengesi suyun kendi kendine iyonlaşması, aşırı iyonların reaksiyona girmesiyle ters yönde hareket edecektir. H iyonları3Ö+, konsantrasyonunuzu azaltmak ve çözümü basit hale getirmek.
Bu durumda, pOH pH'dan daha büyük olacaktır. Oda sıcaklığında (25°C), pH > 7 ve pOH < 7.

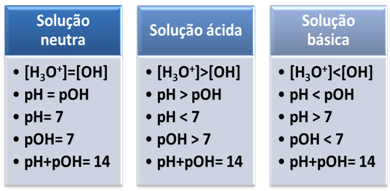
Kısaca:
Jennifer Foğaça tarafından
Kimya mezunu

