Ö fazlar diyagramı bir maddenin herhangi bir zamanda hangi fiziksel durumda olduğunu, sıcaklığını ve basıncını bilerek tanımlamanıza izin veren bir grafiktir.
Belirli bir maddenin faz diyagramını oluşturmak için laboratuvar ölçümleri kullanılır.
Diyagram, katı, sıvı ve buhar durumunu temsil eden üç bölgeye ayrılmıştır.
Bu bölgeleri sınırlayan çizgiler üzerindeki noktalar, maddenin iki halde olabileceği sıcaklık ve basınç değerlerini gösterir.
Bir faz diyagramı aşağıdaki unsurlara sahiptir:
- eğrisi Füzyon: katı ve sıvı durumlara karşılık gelen alanları ayırır.
- eğrisi buharlaşma: sıvı ve buhar fazlarına karşılık gelen alanları ayırır.
- eğrisi süblimasyon: katı ve buhar fazlarına karşılık gelen alanları ayırır.
- üçlü nokta: üç eğrinin kesişme noktası (füzyon, buharlaşma ve süblimasyon). Bu nokta, maddenin aynı anda üç durumda olabileceği sıcaklık ve basınç değerlerini gösterir.
- Kritik nokta: maddenin buhar olduğu en yüksek sıcaklığı gösterir. Bu noktadan sonra sıvı ve buhar halleri arasında ayrım yapmak artık mümkün değildir. Kritik noktanın üzerindeki sıcaklıklarda madde gaz haline gelir.
Aşağıdaki şekilde, bir faz diyagramının bir temsilini sunuyoruz:

da daha fazlasını oku: Fiziksel durum değişiklikleri.
erime eğrisi
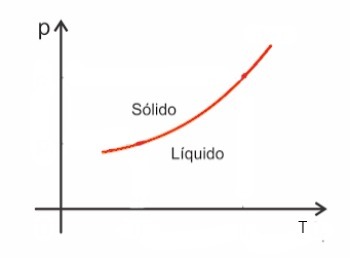
Maddeler genel olarak füzyona girdiklerinde hacimleri artar, katılaştıklarında ise hacimleri azalır. Sonuç olarak, basınçtaki bir artış, erime noktasında (erime sıcaklığı) bir artışa yol açar.
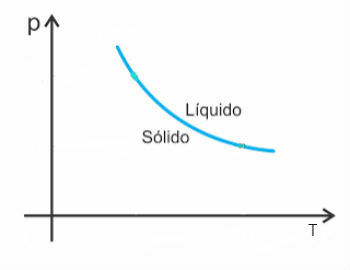
Ancak, erimede hacmi azalan su arasında bazı istisnalar vardır. Bu durumda, basınçtaki bir artış, erime noktasında bir azalmaya neden olur.
Böylece, bu maddelerin erime eğrisi şöyle görünecektir:
Misal
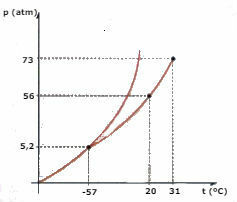
CO faz diyagramını düşünün2 (karbondioksit) aşağıda temsil edilmektedir ve soruları cevaplayınız:
a) CO hangi fazdadır?2 , sıcaklığınız -60 °C ve basınç 50 atm olduğunda?
b) Belirli bir miktarda CO2 sıvı 56 atm basınca maruz bırakılır ve bir kap içinde hapsedilir. Basınç sabit tutularak sıvı ısıtılırsa, buharlaşmanın gerçekleşeceği sıcaklık değeri nedir?
c) CO'nun üçlü noktasının sıcaklık ve basınç değeri nedir?2?
d) Bir parça kuru buz (CO2) 2 atm basınca maruz kalır. Sabit basıncı koruyarak ısıtılır. Belirli bir anda bir faz değişikliği oluşmaya başlar. Bu değişikliğin adı nedir?
çözüm:
a) Diyagramı inceleyerek, CO'nun2 katı fazda olacaktır.
b) Sıcaklık 20°C'ye ulaştığında buharlaşma meydana gelir.
c) Üçlü nokta, CO durumunda, üç eğrinin kesişimine karşılık gelir.2, -57°C sıcaklığa ve 5,2 atm basınca sahip olduğunda, üç fiziksel durum bir arada var olabilir.
d) Süblimleşme gerçekleşir
Daha fazlasını öğrenmek için şunu da okuyun:
- Katılaşma
- Erime ve kaynama noktası
- buharlaşma
- yoğunlaşma
Çözülmüş Alıştırmalar
1) Düşman - 2000
Bugün bile insanların, suyu çevre sıcaklığından daha düşük bir sıcaklıkta muhafaza etmek için toprak kaplar (kavanozlar veya sırsız seramik kaplar) kullanması çok yaygındır. Bunun nedeni ise:
a) Kil suyu ortamdan izole eder, her zaman straformuş gibi kendi sıcaklığından daha düşük bir sıcaklıkta tutar.
b) Kil, kimyasal bileşimi nedeniyle suyu “dondurma” gücüne sahiptir. Reaksiyonda su ısı kaybeder.
c) Kil gözeneklidir ve suyun içinden geçmesine izin verir. Bu suyun bir kısmı buharlaşır, moringadan ısı alır ve suyun geri kalanı daha sonra soğutulur.
d) kil gözeneklidir ve suyun sürahinin dışına yerleşmesine izin verir. Dışarıdaki su her zaman içeriden daha yüksek bir sıcaklıktadır.
e) Moringa, suyun sıcaklığını doğal olarak azaltan higroskopik maddeler salan bir tür doğal buzdolabıdır.
Alternatif c: kil gözeneklidir ve suyun geçmesine izin verir. Bu suyun bir kısmı buharlaşır, moringadan ısı alır ve suyun geri kalanı daha sonra soğutulur.
2) İtalya - 2013
Aşağıdaki şekilde şematik olarak temsil edilen varsayımsal faz diyagramını göz önünde bulundurun:

A, B, C, D ve E noktaları neyi temsil eder?
A noktası: süblimasyon noktası
B noktası: üçlü nokta
C noktası: erime/katılaşma noktası
D noktası: buharlaşma/yoğuşma noktası
E noktası: kritik nokta
3) UECE - 2009
Aşağıda gösterilen PT faz şemasına bakın. Süblimleşme sürecinden geçen bir maddenin yörüngeyi takip ettiği sonucuna varılabilir:

a) X veya Y
b) Y veya U
c) U veya V
d) T veya X
Alternatif b: Y veya U