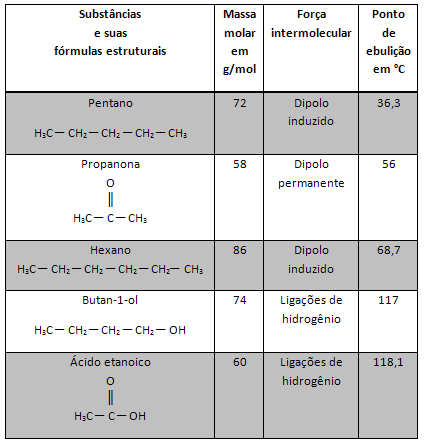
şunu not edebiliriz Bir kimyasal reaksiyona katılan reaktanlardan birinin veya tamamının konsantrasyonunu her arttırdığımızda, gelişme hızında, yani reaksiyonun hızında bir artış olur.
Bunun tersi de doğrudur. Örneğin, şu anda normal alkol yerine alkollü jel kullanmamız tavsiye ediliyor, çünkü daha az yanma riski var ve bu nedenle kazaları önlüyor. Sıradan sıvı alkol aslında daha az miktarda alkol içeren jel alkol ile alkol ve su karışımıdır. Bu nedenle, alkol durumunda, yanma reaktanlarından birinin konsantrasyonu azaldığında, reaksiyon daha yavaş ilerler. Öte yandan, alkol ne kadar saf olursa, yanma reaksiyonu o kadar hızlı olur.

Metinde belirtildiği gibi Kimyasal Reaksiyonların Oluşma Koşulları, bir reaksiyonun gerçekleşmesi için koşullardan biri, etkili çarpışma parçacıklar arasında. Böylece, reaktiflerin konsantrasyonundaki artış, aynı alana hapsedilmiş daha fazla miktarda partikül veya moleküle sahip olmayı mümkün kılar. Bu, aralarındaki çarpışma miktarını arttırır ve ayrıca reaksiyonun meydana gelmesiyle sonuçlanacak etkili çarpışmaların meydana gelme olasılığını arttırır. Sonuç, reaksiyonun daha hızlı gerçekleşmesidir.
Şimdi durma... Reklamdan sonra devamı var ;)
Bunu görmek için şu örneği düşünün: yanan bir korumuz olduğunda ve bu yanmanın daha hızlı işlemesini istediğimizde, kor üfler miyiz yoksa havalandırır mıyız? Bu neden işe yarıyor?
Bu yanma reaksiyonundaki reaktanlardan biri havadaki oksijendir. Salladığımızda hava akımı yanma sırasında oluşan külü uzaklaştırır ve bu da oksijenin kor ile temasını kolaylaştırır. Bu sayede reaktanlar arasındaki teması artırıyor ve yanma reaksiyonunu hızlandırıyoruz.
Kısaca elimizde:

Gazlarla çalışırken, reaktanların konsantrasyonunu arttırmanın bir yolu, basıncı düşür. Bunu yaptığımızda hacmi azaltıyoruz ve sonuç olarak reaktif konsantrasyonlarında bir artış oluyor.

Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Reaktiflerin Konsantrasyonu ve Reaksiyonların Hızı"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/concentracao-dos-reagentes-velocidade-das-reacoes.htm. 27 Haziran 2021'de erişildi.