hibridizasyon sayısını artıran bir fenomen olan tamamlanmamış atomik orbitallerin birleşmesine veya birleşmesine verilen addır. kovalent bağlar bir atomun yapabileceği şey. Yörüngenin, bir elektron bulma olasılığının daha yüksek olduğu atom bölgesi olduğunu hatırlamak.
Bir atomun yaptığı bağların sayısını bilmek ve fenomenini anlamak hibridizasyon, atom hakkında bazı temel noktaları bilmek gerekir:
1Ö nokta: enerji alt seviyeleri
Bir atomun sahip olabileceği enerji alt seviyeleri s, p, d, f'dir.
2Ö nokta: alt düzey başına yörünge sayısı
Aşağıda görebileceğimiz gibi, her bir enerji alt seviyesinin farklı miktarda yörüngesi vardır:
Alt düzey s: 1 yörünge;
p alt seviye: 3 yörünge;
Alt seviye d: 5 yörünge.
Bu yörüngelerin genel gösterimi şu şekilde yapılır:
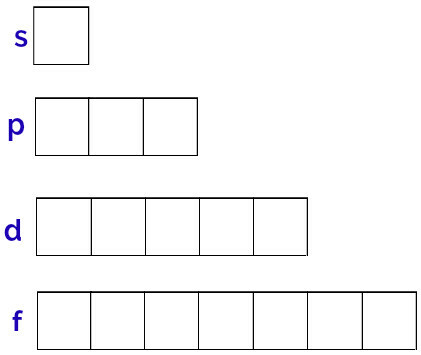
Her alt seviyenin yörüngelerinin temsili
Pauli'ye göre, bir yörünge en fazla 2 elektrona sahip olabilir. döner (dönme hareketleri) ters.
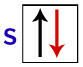
s orbitalinin elektronlarıyla temsili
Hund'a göre, bir alt seviyenin yörüngesi ikinci elektronunu ancak o alt seviyenin diğer tüm yörüngeleri zaten ilk elektronu aldığında alır.
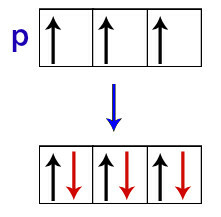
p alt seviye orbitallerinde elektronların dağılımı
3Ö nokta: elektronik dağıtım
Hibritleşmeyi ve bir atomun yaptığı bağ sayısını anlamak için, elektronik dağıtım Linus Pauling diyagramında.

Linus Pauling diyagramı
Her bir alt seviyedeki maksimum elektron sayısının:
s = 2 elektron;
p = 6 elektron;
d = 10 elektron;
-
f = 14 elektron.
Şimdi durma... Reklamdan sonra devamı var ;)
Bu kısa incelemeden sonra artık tanımlayabiliriz. hibridizasyon nedir. Bunun için bor kimyasal elementini kullanacağız (atomik numara = 5) örnek olarak.
Elektronik bor dağıtımı yaptığımızda:
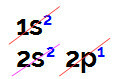
Linus Pauling diyagramında elektronik bor dağılımı
Borun s alt seviyesinde 2, p alt seviyesinde ise 1 elektrona sahip olduğunu bu dağılımda gözlemlemek mümkündür. değerlik katmanı.
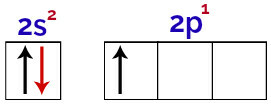
Bor değerlik tabakasının yörüngelerindeki elektronlar
Bor, 1 tamamlanmamış yörüngeye sahip olduğundan, bağ sayısı her zaman doğrudan tamamlanmamış yörünge sayısıyla ilişkili olduğundan, yalnızca bir kovalent bağ yapmalıdır.
Böylece bor atomu dış ortamdan enerji aldığında özellikle değerlik kabuğundaki elektronları uyarılır. Bu, s orbitalinden gelen elektronlardan birinin boş p orbitallerinden birini terk etmesine ve işgal etmesine neden olur, böylece aşağıdaki resimde görebileceğiniz gibi 3 eksik atomik orbital ile sonuçlanır:

Bor atomunun uyarılmış halinin temsili
Son olarak, tamamlanmamış p orbitalleri ile tamamlanmamış s orbitalinin birleşimi vardır. Bu birliğin adı hibridizasyon. Bir s orbitalinin iki p ile kaynaşmasına sahip olduğumuz için buna denir. hibridizasyon sp2.
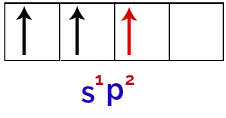
Bor atomunda hibritleştirilmiş orbitallerin temsili
Bora ek olarak, kükürt (S), Ksenon (Xe), fosfor (P), karbon (Ç), berilyum (Ol).
Benden Diogo Lopes Dias
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
GÜNLER, Diogo Lopes. "Hibridizasyon nedir?"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-hibridizacao.htm. 27 Haziran 2021'de erişildi.
Bağlanma enerjisi, Kimyasal reaksiyonlar, bağları koparma, enerji değişiminin incelenmesi, reaksiyonların entalpi değişimi, enerji temini, reaktiflerin bağlantısının kopması, endotermik süreç, enerji salınımı, oluşum