Ametaller, elektron kazanma ve anyon oluşturma eğiliminde olan elementlerdir (negatif yüklü türler). Bu, taburcu oldukları anlamına gelir.elektronegatiflikveya elektronları çekme eğilimi yüksektir. Bir metal ne kadar elektronegatifse, o kadar reaktif olur diyoruz.
Deneysel olarak, aşağıdaki şekilde verilen metal olmayanların reaktivite sırasını belirlemek mümkün olmuştur:
F > O > N > Cℓ > Br > I > S > C > P > H
Sırasıyla elektronegatiflik değerlerine bakın:
4,0 > 3,5 > 3,0 > 3,0 > 2,8 > 2,5 > 2,5 > 2,5 < 2,1
Bunu süslemek için bir çeşit "hile" var. metal olmayanların elektronegatiflik sırası, her kelimenin baş harfinin söz konusu elementlerin sembolüne karşılık geldiği aşağıdaki cümle ile verilmektedir:
“FSelam Öyok NÖ Clübe, brBende var DIR-DİRah Çölmek Piçin Hhastane"
Ama neden metal olmayanların reaktivitesini bilmemiz gerekiyor? Bunun bir nedeni, kimyasal reaksiyonun gerçekleşip gerçekleşmeyeceğini belirlemektir.
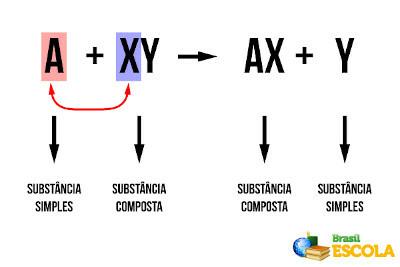
at basit değişim veya yer değiştirme reaksiyonları Basit bir maddenin (sadece bir tür kimyasal element tarafından oluşturulan) bir madde ile reaksiyona girdiği maddelerdir. bileşik madde ve o maddenin elementlerinden birinin yerini alarak yeni bir basit madde ve diğerini oluşturur. oluşur. Genel olarak, elimizde:

Genel Yer Değiştirme Reaksiyonu
“A”nın “Y”yi değiştirdiğini ve “X”e katıldığını görün. Bu da bir Redoks reaksiyonu, elektron transferi olduğu için. "A" ve "Y"nin metal olmadığı göz önüne alındığında, "A"nın elektron kazanarak (indirgenerek) bir anyon oluşturduğunu ve "AX" bileşik maddesinin bir parçası olduğunu elde ederiz. Öte yandan, “XY” bileşik maddesindeki bir anyon olan “Y”, elektronlarını kaybetti (oksidasyona uğradı) ve yeni “Y” basit maddesini oluşturdu.
Şimdi durma... Reklamdan sonra devamı var ;)
Bu tür bir reaksiyon meydana geldiğinde, elementin olup olmadığını görmek için metal olmayanların reaktivitesini analiz etmek gerekir. Basit maddenin yüzdesi, ametali maddeden ayırmak için gerekli reaktiviteye sahip olacaktır. oluşur. Örneğin, flor ve sodyum klorür arasındaki reaksiyonu düşünün:
F2(sulu) + 2 NaCl(İşte) → ?
Florür mü (F2) kloru sodyum klorürden (NaCl) uzaklaştırabilir ve sodyum ile yeni bir bileşik oluşturabilir mi? Metal olmayanların reaktivite hattında flor, klordan daha reaktiftir. Böylece kloru NaCl'den ayırmayı başarır ve reaksiyon aşağıdaki gibi gerçekleşir:
F2(sulu) + 2 NaCl(İşte) → 2 NaF(İşte) + Cl2(sulu)
Daha elektronegatif olduğundan, F2(sulu) indirgenir ve her flor atomu bir elektron kazanarak F anyonunu oluşturur.-(İşte). Bu anyon, Na katyonu ile iyonik bir bağ oluşturur.+(İşte), sodyum florür (NaF) üretiyor. Bu arada, Cl anyonu-(İşte)Sodyum klorürün (NaCl) bir parçası olan, oksitlenmiş ve basit madde Cl'yi birleştiren ve oluşturan klor atomlarını oluşturmuştur.2.
Şimdi aşağıda başka bir örneğe bakın. Bu reaksiyon gerçekleşecek mi?
ben2(sulu) + KCl(İşte) → ?
Ametallerin reaktivite sırasına bakarsak, gerçekleşmeyecek Cl I'den daha reaktif olduğu için bu maddeler arasında redoks reaksiyonu yoktur, bu nedenle I2 Cl'yi KCl maddesinden çıkarmak için gerekli güce sahip olmayacaktır.
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Metal olmayanların reaktivite sırası"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/ordem-reatividade-dos-ametais.htm. 28 Haziran 2021'de erişildi.