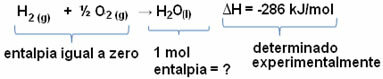
Atom veya iyon, yalnızca iyonlaşma enerjisi olan yeterli enerjiyi alırsa elektron kaybeder.
Pratikte, en önemli şey ilk iyonlaşma potansiyeli veya ilk iyonlaşma enerjisi, bu, ilk elektronun çıkarılmasına karşılık gelir. Bu elektron çekirdekten en uzak olduğu için genellikle en düşük iyonlaşma enerjisidir. çekirdeğe olan çekim gücü en düşüktür, daha az enerji gerektirir ve daha kolaydır onu kaldır.
Ayrıca elektron kaybıyla atom yarıçapı azalır ve iyon giderek daha pozitif hale gelir, dolayısıyla atomla çekim artar. çekirdek güçlenir ve sonuç olarak bir sonraki elektronu çekmek için daha fazla enerjiye ihtiyaç duyulur ve böylece art arda.
Örneğin, sodyum atomunun ilk iyonlaşma enerjisi 406 kJ/mol değerindedir. İkinci iyonlaşma enerjisi 4560'tır, yani birincisinden çok daha yüksektir. Bu, sodyumun iki elektron çekmesinin tek bir elektrondan çok daha fazla enerji gerektirdiğini gösterir. Bu nedenle doğada +1 yüklü sodyum atomları bulmak daha yaygındır.
Aşağıdaki alüminyum durumunda bunun nasıl olduğuna dikkat edin:
13Al+ 577.4 kJ/mol → 13Al1++ ve-
13Al+ 1816.6 kJ/mol → 13Al2++ ve-
13Al+ 2744.6 kJ/mol → 13Al3++ ve-
13Al+ 11575.0 kJ/mol → 13Al4++ ve-
Böylece, Alüminyum için aşağıdaki iyonlaşma enerjisi sırasına (EI) sahibiz:
Şimdi durma... Reklamdan sonra devamı var ;)
1. EI < 2. EI < 3. EI <<< 4. EI
Bu gerçeklerden şu sonucu çıkarabiliriz:

Bu nedenle, periyodik tablonun aynı ailesindeki veya aynı periyodundaki elementleri düşünürsek, Atom numaraları arttıkça iyonlaşma enerjileri azalır, çünkü elektronlar çekirdekten uzaklaştıkça onlar. Bu şekilde iyonlaşma enerjisi periyodik cetvelde aşağıdan yukarıya ve soldan sağa doğru büyür. Bu nedenle iyonlaşma enerjisi periyodik bir özelliktir.
Bunun aşağıda nasıl gösterildiğine bakın ve bazı atomların deneysel olarak kJ (kilojoule) cinsinden elde edilen ilk iyonlaşma enerjisinin değerlerini karşılaştırın:

Periyodik Tablonun ikinci periyodundaki elementlerin iyonlaşma enerjisi değerlerinin üçüncü periyottakilerden nasıl daha büyük olduğuna dikkat edin, vb. Ayrıca 1A ailesinin elemanlarının ilk iyonlaşma enerjilerinin 2A'nınkinden daha düşük olmasına vb. dikkat edin.
Düşük iyonlaşma enerjisine sahip olan bu temsili elementler, kararlı hale gelmek, yani soy gaz konfigürasyonuna sahip olmak için elektronlarını kaybederler. İyonlaşma enerjisi yüksek olanlar (ametaller) elektronları kaybetmek yerine alırlar.
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "İyonlaşma enerjisi"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/energia-ionizacao.htm. 28 Haziran 2021'de erişildi.