at moleküller arası kuvvetler, genel olarak adlandırılan Van der Waals Kuvvetleri, Üç vardır: indüklenmiş dipol ile indüklenen dipol, hidrojen bağları ve kalıcı dipol-kalıcı dipol. Bu metinde, bu üç kuvvetten yalnızca sonuncusunu ele alacağız:
Güç kalıcı dipol-kalıcı dipol, ya da sadece, dipol-dipol sadece oluşur polar molekülleryani, yüzeyi boyunca düzgün bir yük dağılımına sahip olmayanlar. Bir örnek vermek gerekirse, HCl (hidroklorik gaz) molekülünde elektronik bulut, hidrojenden daha elektronegatif olduğu için klor atomuna doğru daha fazla yer değiştirir.
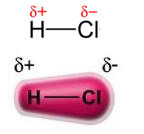
Klor atomunun çevresinde bir elektron birikimi olduğuna dikkat edin, bu da bir klor atomunun oluşumuna neden olur. negatif kutupYunan harfi delta ile sembolize edilen (-δ). Sonuç olarak, hidrojen atomunun etrafındaki bölgede bir pozitif kutup (+δ), Düşük elektronik yoğunluğa sahip olduğu için. HCl molekülü daha sonra bir elektrik dipol ve bu nedenle, diğer komşu HCl molekülleri ile temas ettiğinde, aşağıda görülebileceği gibi, moleküllerin zıt kutupları arasında bir çekim kuvveti vardır:
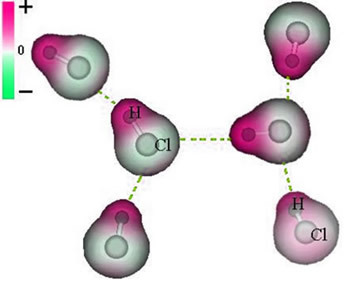
Bir molekülün dipolünün negatif ucu ile diğer bir molekülün dipolünün pozitif ucu arasında kurulan bu çekim kuvveti, dipol-dipol kuvvetini oluşturur..
Yani adından da anlaşılacağı gibi dipol kalıcıdır, bu yüzden sadece polar bileşiklerde oluşur. Ve bir molekülün polaritesi ne kadar yüksek olursa, maddedeki dipol-dipol etkileşimleri o kadar yoğun olur.
Katı fazda ise, kalıcı dipol oluşumu, her molekülün uzaydaki konumunu yönlendirir. dipolar kristaller; aşağıda gösterilen hidrojen bromür durumunda olduğu gibi:
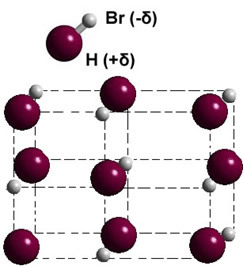
Molekülleri arasında dipol-dipol kuvvetine sahip olan diğer polar madde örnekleri şunlardır: H2S, CO, HCCI3, SADECE2.
Bu moleküller arası kuvvet, orta yoğunlukindüklenmiş dipol kaynaklı dipol çekim kuvvetinden daha güçlü, ancak hidrojen bağından daha az yoğun olduğu için. Bu nedenle erime ve kaynama noktaları, indüklenmiş dipol kuvvetine sahip maddelerden daha yüksektir. Kalıcı dipol kuvveti daha güçlü olduğundan, moleküllerinin etkileşimlerinin bozulması için daha fazla enerji sağlamak gerekir.
Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/forca-intermolecular-dipolo-dipolo.htm
