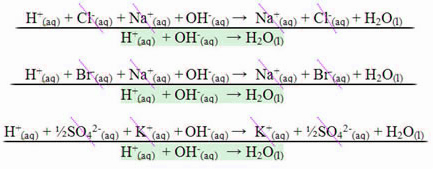bu aktivasyon enerjisi uygun bir yönelimde yapılan reaktan partiküller arasındaki çarpışmanın gerçekleşmesi ve bir reaksiyonla sonuçlanması için gereken minimum enerji miktarıdır.
Reaksiyonlar yalnızca, reaktanlar aktivasyon enerjisine (veya reaksiyondan reaksiyona değişen gerekli minimum enerjiye) sahip olduğunda meydana gelir; miktar veya biçimde) veya kendilerine tedarik edildiğinde.
Örneğin, metalik sodyum su ile temas ettiğinde şiddetli reaksiyona girer. Bu, bu reaktanların enerji içeriğinin reaksiyonun gerçekleşmesi için zaten yeterli olduğu anlamına gelir.
Bir sobanın açılması durumunda, yanma reaksiyonu, yalnızca soba tarafından salınan gazın yanına yanan bir kibrit veya başka bir ateş kaynağı yerleştirirsek gerçekleşir. Demek ki bu durumda aktivasyon enerjisine ulaşması ve reaksiyonun gerçekleşmesi için sisteme enerji verilmesi gerekiyordu.
Fosforun kendisinin kullanılması durumunda, yanması için aktivasyon enerjisi sürtünme ile sağlanır. Aynı şey, içinde bulunan gazın yanması için gerekli aktivasyon enerjisini veren bir kıvılcıma ihtiyaç duyan çakmaklarda da olur.
Aktivasyon enerjisi, hidrojen peroksitin ayrışmasında olduğu gibi ışıkla da sağlanabilir. Bu yüzden koyu veya opak şişelerde saklanır.
Şimdi durma... Reklamdan sonra devamı var ;)

Böylece, aktivasyon enerjisinin (E) olduğu sonucuna varabiliriz.a kadar) reaksiyonun başlaması için gereken enerji (E) ile reaktanların içerdiği enerji (E) arasındaki farktır.pr):

Aktivasyon enerjisi, reaksiyonun gerçekleşmesi için bir engeldir ve reaktanların bağlarını kırmak için gereklidir. Bununla reaksiyon gerçekleşir ve ürünleri oluşturmak için yeni bağlantılar yapılır.
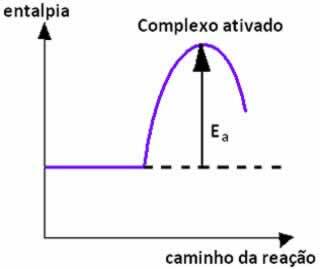
Uygun yönelimli reaktant parçacıkları arasındaki çarpışma eşit enerji veya aktivasyon enerjisinden daha yüksek, ürünlerin oluşumundan önce ara ve kararsız bir durum oluşur, mezhep karmaşık aktif, reaktan bağlarının zayıfladığı ve ürün bağlarının oluştuğu. Böylece, aktivasyon enerjisi, aktifleştirilmiş kompleksi oluşturmak için gereken enerjidir.
Aşağıda, reaksiyonun gerçekleşmesi için bir engel olarak aktivasyon enerjisini gösteren bir grafiğimiz var:
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Aktivasyon enerjisi"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/energia-ativacao.htm. 27 Haziran 2021'de erişildi.