Spor faaliyetlerinde, hastanelerde ve günlük hayatımızda sıcak ve soğuk anlık kompres kullanımı oldukça yaygındır. Her iki durumda da belirli maddeler su ile reaksiyona girer. Örneğin, soğuk kompres durumunda, suyu NH'den ayıran iki kapsül içerir.4ŞEHİR3, suda çözündüğünde ısıyı emer ve anında soğuk üretir. Sıcak kompres durumunda CaCl suda çözünür2 veya MgSO4, hangi enerji üreten ısıyı serbest bırakır.
Fakat neden bazı çözeltiler ekzotermik olduğundan ısı yayar; ve diğerleri endotermik olarak emilir mi?
Peki, bu konuyu anlamak için çözeltilerin entalpi değişimi (ΔH), iki adımdan oluşur:
(1.) Retiküler entalpi (ΔHgeri): Bir çözünen suda çözündüğünde, ilk adım kristal kafes içindeki iyonlarını ayırmaktır. İyonlar arasındaki bağları kırmak için sisteme enerji sağlamak gerekir. Yani bu ilk süreç endotermik, enerjiyi emdiği için; senin olmak pozitif entalpi (ΔH > 0).
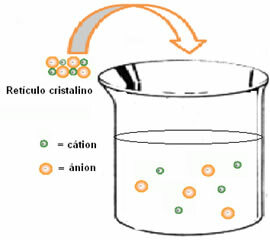
(2.) Hidrasyon entalpisi (ΔHsaklanmak): iyonlar ayrıldıktan sonra çözücü molekülleri tarafından sarılırlar. Su söz konusu olduğunda çözücüdür ve hidrasyonun gerçekleştiğini söylüyoruz. Suyun dipolleri sırasıyla zıt yüklü iyonlar tarafından çekilir; bu nedenle, bu etkileşimin gerçekleşmesi için enerjinin serbest bırakılması gereklidir. Böylece hidratasyonda
entalpi negatif olacaktır (ΔH < 0), çünkü süreç ekzotermik.Şimdi durma... Reklamdan sonra devamı var ;)
Aşağıdaki şekil, iyon-dipol etkileşiminin, yani ayrılmış iyonların yükleri ile su dipolü arasındaki çekimin olduğu hidrasyonun nasıl gerçekleştiğini göstermektedir:
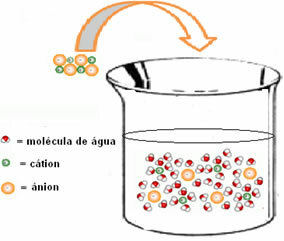
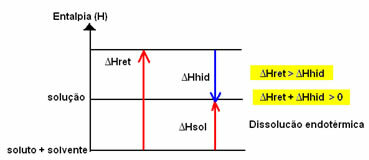
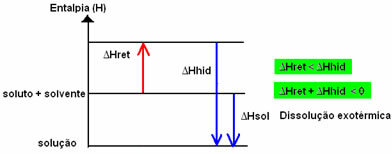
Çözeltinin entalpi değişimi (ΔHGüneş) bu iki entalpinin toplamı ile belirlenecektir. Sonuç pozitifse, retiküler entalpinin daha yüksek olduğu anlamına gelir, bu nedenle çözünme entalpisi işlemin endotermik olduğunu gösterecektir.
Endotermik bir çözünmenin entalpi diyagramı aşağıda gösterilmiştir:
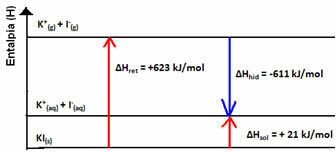
Bu, aşağıda gösterilen potasyum iyodür çözünmesi durumunda gösterilir:
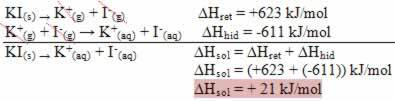
Entalpi diyagramınız şu şekilde temsil edilecektir:
Sonuç pozitifse, hidratasyon entalpisi retiküler olandan daha büyük olacaktır ve süreç ekzotermiktir. Ekzotermik çözünmelerin entalpi diyagramları aşağıdaki örnekte gösterildiği gibi temsil edilir:
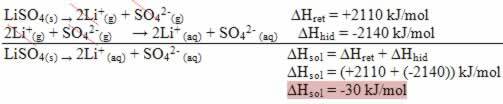
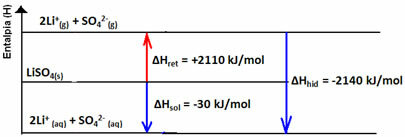
Aşağıdaki entalpi diyagramınızı not edin:
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Çözüm Entalpi Varyasyonu"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/variacao-entalpia-solucao.htm. 28 Haziran 2021'de erişildi.



