bu İlkYasaverirTermodinamik bir uygulamasıdır prensipverirkorumaverirenerji termodinamik sistemler için. Bu kanuna göre, değişken içsel enerji bir termodinamik sistemin miktarı arasındaki farktır. sıcaklık sistem ve onun yaptığı iş tarafından emilir.
BakAyrıca:Termolojinin temel kavramları ve özeti
Termodinamiğin Birinci Yasası nedir?
Termodinamiğin Birinci Yasası, enerjinin korunumu ilkesinin doğrudan bir sonucudur. Bu ilkeye göre, bir sistemin toplam enerjisiher zaman sabit kalır, çünkü o kaybolmaz, dönüşür.
Kapsamında Termodinamik, kullanılmış daha spesifik kavramlar ve enerji tasarrufu ilkesinde kullanılanlardan daha az geneldir. Termodinamiğin Birinci Yasasında aşağıdaki gibi kavramları kullanırız: enerjiiç,sıcaklık ve işkapsamı ile ilgili olan, Termal makineler (Termodinamik için temel öneme sahip teknolojik uygulamalar).

Buharla çalışan bir makine hayal edin, bu makinenin çalışma sıvısı (su buharı) harici bir kaynaktan ısı aldığında, iki enerji dönüşümü mümkündür: buharın kendi
sıcaklık birkaç derece arttırılabilir, hatta genişletmek ve o makinenin pistonlarını hareket ettirerek belirli bir miktarda iş."Bir termodinamik sistemin iç enerjisindeki değişim, onun tarafından emilen ısı miktarı ile bu sistemin yaptığı iş miktarı arasındaki farka karşılık gelir."
Termodinamiğin Birinci Yasasının Formülü
Termodinamiğin Birinci Yasasını matematiksel olarak tanımlamak için kullanılan formül aşağıda gösterilmiştir:

sen – iç enerji değişimi (cal veya J)
S – ısı (kireç veya J)
τ – iş (kireç veya J)
Bu formülü kullanabilmek için bazı sinyal kurallarına dikkat etmemiz gerekiyor:
ΔU – sistem sıcaklığı artarsa pozitif olacaktır;
ΔU – sistem sıcaklığı düşerse negatif olacaktır;
S – sistem dış ortamdan ısı çekiyorsa pozitif olacaktır;
S – sistem dış ortama ısı verirse negatif olur;
τ – sistemin genişlemesi, dış çevre üzerinde çalışma yapılması olumlu olacaktır;
τ – sistem sözleşme yaparsa, dış ortamdan iş alırsa olumsuz olacaktır.
iç enerji değişimi
ΔU terimi, enerjiye atfedilen enerji değişimini ifade eder. kinetik enerji Sistemi oluşturan parçacıkların bir ideal gaz durumunda, ΔU'nun şuna eşdeğer olduğu söylenebilir:
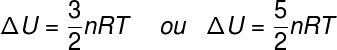
Hayır – mol sayısı (mol)
$ – ideal gazların evrensel sabiti (0.082 atm.l/mol. K veya 8.31 J/mol. K)
T – mutlak sıcaklık (kelvin)
Formüller incelendiğinde, sistemde sıcaklık değişimi yoksa, içsel enerji da değişmeden kalacaktır. Ayrıca döngüler halinde çalışan termal makineler için şunu da söylemek önemlidir. her döngünün sonunda iç enerjinin değişimi sıfır olmalıdır., çünkü bu noktada motor ilk sıcaklıkta çalışmaya geri döner.
BakAyrıca:Termal makinelerin performansı: nasıl hesaplanır?
Sıcaklık
Sisteme aktarılan ısı miktarını ifade eden bir sonraki terim olan Q'ya geçerken, genellikle kalorimetrinin temel denklemi, aşağıda gösterilen:
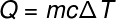
S -ısı (kireç veya J)
m – kütle (g veya kg)
ç – özgül ısı (cal/gºC veya J/kg. K)
ΔT – sıcaklık değişimi (santigrat veya kelvin)
İş
Termodinamiğin Birinci Yasası ile ilgili niceliklerin sonuncusu iş (τ)'dir. sadece sabit basınç altında meydana gelen dönüşümler için analitik formül, ayrıca bilinen sevmek izobarik dönüşümler, izlemek:
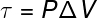
P – basınç (Pa veya atm)
ΔV – hacim değişimi (m³ veya l)
Sisteme uygulanan basınç sabit olmadığında, iş, basınç-hacim grafiğinin alanı (P x V) ile hesaplanabilir. Bu skaler büyüklük hakkında daha fazla bilgi edinmek için şu adresi ziyaret edin: iş.
çözülmüş alıştırmalar
Soru 1)(CefetMG) Kapalı bir ısıl çevrimde yapılan iş 100 J'ye eşittir ve ısıl değişimlerde yer alan ısı, sıcak ve soğuk kaynaklarla sırasıyla 1000 J ve 900 J'ye eşittir.
Termodinamiğin Birinci Yasasından, bu termal döngüdeki iç enerjinin joule cinsinden değişimi şöyledir:
a) 0
b) 100
c) 800
d) 900
e) 1000
çözüm
Alternatif a.
Egzersizi Termodinamiğin Birinci Yasasını kullanarak çözelim, not edin:

Açıklamaya göre, kapalı bir termodinamik çevrimde iç enerjinin değişimini hesaplamamız isteniyor, bu durumda biliyoruz ki, Makine, çevrimin başlangıcında olduğu gibi aynı sıcaklıkta çalışmaya geri döneceğinden, iç enerji değişimi sıfır olmalıdır.
Soru 2)(Üf) Bir ideal gaz örneği, izobarik ve adyabatik dönüşüm sırasında hacmini iki katına çıkararak genişler. Gazın maruz kaldığı basıncın 5.10 olduğunu düşünürsek6 Pa ve ilk hacmi 2.10-5 m³ diyebiliriz:
a) İşlem sırasında gazın emdiği ısı 25 cal'dir.
b) Gazın genleşmesi sırasında yaptığı iş 100 cal'dir.
c) Gazın iç enerji değişimi –100 J'dir.
d) Gaz sıcaklığı sabit kalır.
e) Yukarıdakilerin hiçbiri.
çözüm
Alternatif c.
Alıştırma ifadesi tarafından sağlanan bilgileri kullanarak, doğru alternatifi bulmak için Termodinamiğin Birinci Yasasını kullanacağız:
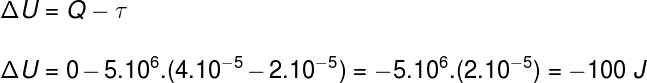
Soru 3)(vay) Bir mutfak bidonunda yüksek basınçlı gaz bulunur. Bu silindiri açtığımızda gazın hızla atmosfere kaçtığını fark ederiz. Bu süreç çok hızlı olduğu için adyabatik bir süreç olarak düşünebiliriz.
Termodinamiğin Birinci Yasasının ΔU = Q - W ile verildiğini düşünürsek, burada ΔU enerjideki değişimdir gazın içinde, Q ısı şeklinde aktarılan enerjidir ve W gazın yaptığı iştir, bu doğru şunu belirtin:
a) Gaz basıncı artar ve sıcaklık azalır.
b) Gazın yaptığı iş pozitiftir ve gazın sıcaklığı değişmez.
c) Gazın yaptığı iş pozitifti ve gazın sıcaklığı azaldı.
d) Gaz basıncı artmış ve yapılan iş negatif çıkmıştır.
çözüm
Alternatif c.
Gaz hacmi genişlediğinde, yapılan işin pozitif olduğunu, yani gazın kendisinin dış ortamda iş yaptığını söylüyoruz. Ayrıca, işlem çok hızlı gerçekleştiği için gazın çevre ile ısı alışverişi yapması için zaman yoktur, dolayısıyla aşağıdakiler meydana gelir:
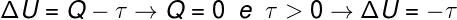
Hesaba göre gazın iç enerjisi yapılan işe eşit miktarda azalır. Ayrıca gazın iç enerjisinde bir azalma olduğu için gazda da bir azalma vardır. sıcaklık.
Soru 4)(Udesc) Bir fizik laboratuvarında, termodinamik analiz amaçları için ideal gaz olarak kabul edilebilecek bir gazla deneyler yapılır. Gazın termodinamik bir işleme tabi tutulduğu deneylerden birinin analizinden, gaza sağlanan tüm ısının işe dönüştürüldüğü sonucuna varıldı.
Temsil eden alternatifi işaretleyin doğru şekilde deneyde gerçekleştirilen termodinamik süreç.
a) izovolümetrik süreç
b) izotermal süreç
c) izobarik süreç
d) adyabatik süreç
e) bileşik süreç: izobarik ve izovolümetrik
çözüm
Alternatif b.
Bir gaza verilen tüm ısının işe dönüşmesi için, gaz tarafından iç enerjinin emilmemesi gerekir. başka bir deyişle, gazın izotermal bir süreçten, yani sıcaklıkta gerçekleşen bir süreçten geçmesi gerekir. sabit.
Rafael Hellerbrock tarafından
Fizik öğretmeni
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/fisica/primeira-lei-da-termodinamica.htm