År 1786 dissekerade den italienska anatomisten Luigi Galvani (1737-1798) en groda på sitt bord, på vilken en elektrostatisk maskin låg. Galvani såg djurets muskler dra ihop sig när hans assistent av misstag rörde spetsen på skalpeln mot grodans lår. Med andra ord hände detta när grodans vävnader berördes av två olika metaller.
Galvani började försvara, från det ögonblicket, en teori som försökte förklara detta faktum: teorin om ”animalisk elektricitet”. Enligt Galvani var metaller bara ledare för elektricitet, som i själva verket skulle finnas i grodans muskler.
Men hans teori var fel och detta sågs av den italienska fysikern Alessandro Volta (1745-1827), som utförde flera experiment och märkte att när plattan och tråden var gjorda av samma metall, uppstod inte kramperna, vilket visade att det inte fanns något flöde av elektricitet. Således fortsatte han med att försvara (rätt) koncept att el inte härrör från grodans muskler utan från metaller och att djurets vävnader ledde denna elektricitet.
För att bevisa att han hade rätt, skapade Volta en krets bildad av en elektrolytisk lösning, det vill säga en lösning med joner upplöst, som han kallade våtledare eller andra klassens ledare, placerad i kontakt med två elektroder metallisk. Dessa sista kallade Alessandro Volta torra ledare eller ledare av första klass.
Han gjorde detta genom att placera en våt ledare (som var en vattenhaltig saltlösning) mellan två torra ledare (som var metaller förbundna med en ledande tråd). I det ögonblicket observerade han att det elektriska flödet vaknade. Han förstod också att beroende på de metaller han använde kunde strömflödet vara större eller mindre. Således kan vi erkänna att tanken på vad en hög är redan förstods och förklarades av Volta.
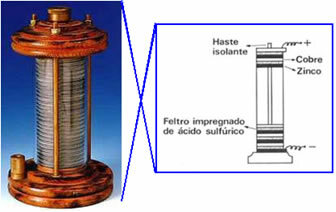
År 1800 skapade Volta den första elektriska cellen, som kom att kallas bakre hög, galvanisk hög eller voltaisk cell och fortfarande, "radband". En schematisk bild av denna hög visas nedan: han placerade en kopparskiva ovanpå en filtskiva som blötläggts i en svavelsyralösning och slutligen en zinkskiva; och så vidare, stapla dessa serier i en stor kolumn. Koppar, filt och zink hade ett hål i mitten och gängades på en horisontell stång, varigenom de var förbundna med en ledande tråd.
Sluta inte nu... Det finns mer efter reklam;)
Detta experiment orsakade omvälvningar i den vetenskapliga världen och därefter alla enheter som producerade el från processer kemikalier (det vill säga som producerade kemisk energi i elektrisk energi) kom att kallas voltaiska celler, galvaniska celler eller, helt enkelt batterier.
Volta gjorde samma experiment med olika metaller och elektrolytlösningar, såsom silver- och zinkskivor åtskilda av saltlösning-blötlagda flanellskivor. Han utförde till och med en demonstration av denna upptäckt för Napoleon Bonaparte, som framgår av figuren nedan, vid vetenskapsakademin i Paris.

Alessandro Volta visar sin upptäckt för Napoleon
En annan Volta experiment med batterier var glasögon, där han placerade två plattor av olika metaller sammankopplade av en ledande tråd, men åtskilda av elektrolytlösningar.
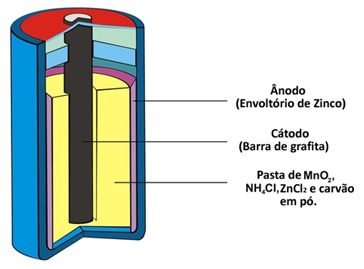
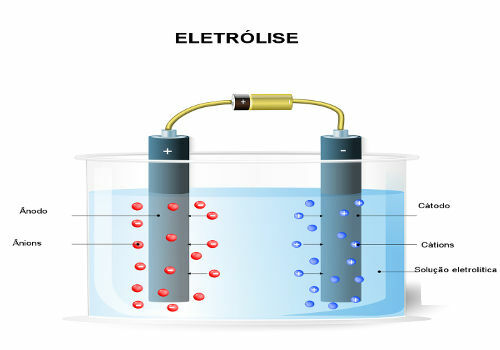
Vi vet för närvarande att det som händer i en cell, som de som skapats av Volta, är att el flyter från polen. negativ, kallas anoden, som oxiderar, förlorar elektroner till den positiva polen, kallad katoden, som minskar, ökar elektroner.
Dessa batterier tillverkade i vattenlösning används inte mycket nuförtiden; bara när det gäller forskning, men de var principen som utvecklade de moderna batterier som vi känner idag som batterier torra och som är mycket mer praktiska att använda och bära, samt ge en tillfredsställande elektrisk ström för mycket mer. tid.
Av Jennifer Fogaça
Examen i kemi