Dynamisk jämvikt eller kemisk jämvikt i en reaktion inträffar när framåt- och bakåtreaktionerna inträffar samtidigt. Dessa så kallade reversibla system representeras av pilar i båda riktningarna:  eller
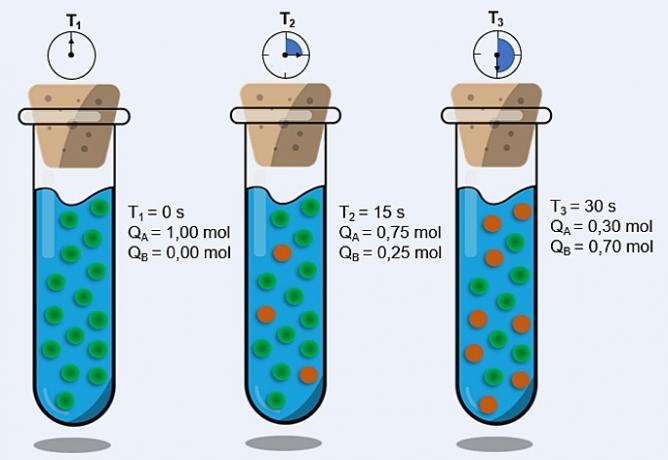
eller  . Ett exempel på en reversibel reaktion nämns i bilden ovan, mellan jodgas och vätgas.
. Ett exempel på en reversibel reaktion nämns i bilden ovan, mellan jodgas och vätgas.
I början av reaktionen är mängden reaktanter maximalt och mängden produkter är noll. Reaktanterna reagerar emellertid med varandra, minskar deras koncentration och ökar de för de bildade produkterna. Utvecklingshastigheten för den direkta reaktionen minskar också.
När koncentrationen av produkterna ökar startar den omvända reaktionen och reaktanterna bildas igen; utvecklingshastigheten för den inversa reaktionen ökar också.
Vid kemisk jämvikt vid konstant temperatur är utvecklingshastigheterna för framåt- och bakåtreaktionerna lika.
Alltdirekt = Alla omvänd
Priserna är desamma, men koncentrationerna inte. Koncentrationerna av reagens och produkter är osannolikt desamma. Endast i sällsynta fall inträffar detta. I de flesta fall kommer koncentrationen av reagens att vara högre än för produkterna eller tvärtom.
Således har vi tre möjliga sätt att grafiskt representera utvecklingshastigheterna för direkta och omvända reaktioner, som relaterar koncentrationerna av reaktanter och produkter över tid. Låt oss titta på varje fall:
1: a fallet: Lika koncentrationer:
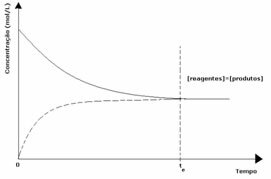
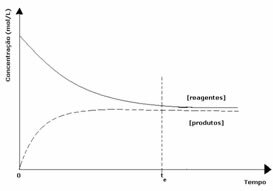
Som framgår av diagrammet, vid tidpunkten toch framåt- och bakåtreaktionerna är desamma, i vilket fall koncentrationerna av reaktanter och produkter är desamma. Således flyttas inte balansen till någon sida, intensiteten för båda reaktionerna är densamma, som uttryckt nedan:
Sluta inte nu... Det finns mer efter reklam;)
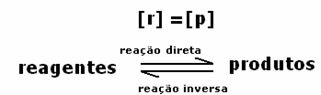
2: a fallet: Koncentration av reagens som är större än koncentrationen av produkter:
I detta fall observeras att när man når jämvikt är koncentrationen av reagens större än för produkterna. Således dras slutsatsen att om det finns mer reaktant sker den inversa reaktionen med större intensitet. Reaktionen flyttas åt vänster:
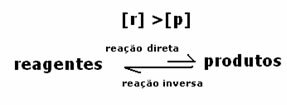
3: a fallet: Koncentration av produkter som är större än reagenser:
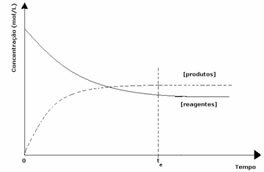
Eftersom koncentrationen av produkter vid jämvikt är större betyder det att reaktionen är flyttas till höger, eftersom den direkta reaktionen (med bildandet av produkter) sker med större intensitet.
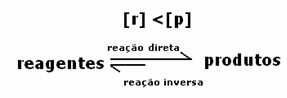
Vad som kommer att indikera om reaktionen tenderar till höger eller vänster kommer att vara jämviktskonstanten K, som bara beror på temperaturen.
Av Jennifer Fogaça
Examen i kemi
Brasilien skollag
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
FOGAÇA, Jennifer Rocha Vargas. "Grafisk studie av kemisk balans"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/quimica/estudo-grafico-equilibrio-quimico.htm. Åtkomst den 28 juni 2021.
Kemi

Testa dina kunskaper och lär dig mer med den här listan över lösta övningar om kemiska balanser. Genom detta material kommer du att kunna bättre förstå hur man arbetar med jämviktskonstanter (Kp, Kc och Ki), jämviktsförskjutning, pH och pOH, liksom jämvikt i så kallade buffertlösningar.