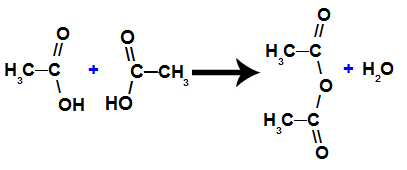
Hydrogenering sker med omättade acykliska kolväten, det vill säga som har öppna kedjor med dubbla eller trippelbindningar, såsom alkener, alkyner och diener. Det kan också förekomma i aromatiska kolväten, eftersom de har dubbelbindningar i ringen och med cyklaner (cykloalkaner) på upp till fem kol.
Dessa föreningar reagerar som vätgas i närvaro av någon katalysator, såsom nickel, platina och palladium, under upphettning. Således inträffar en additionsreaktion, där pi (π) bindningen bryts, bildar två nya enkelbindningar och väte införs i molekylen.
Generellt sett har vi:
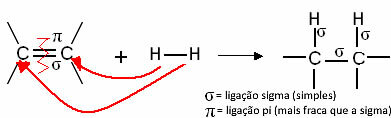
Generisk hydreringsreaktion
Låt oss nu titta på några exempel:
- Hydrogenering till alkener: Den erhållna produkten är en alkan.
Nedan har vi en hydreringsreaktion av eten (eller eten) för att erhålla etan:
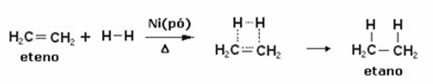
Exempel på en etylenhydreringsreaktion
Denna typ av katalytisk hydrering används av livsmedelsindustrin för att framställa halvfasta fetter såsom margariner. Vegetabiliska oljor och fetter skiljer sig endast genom att oljor har långa molekyler med dubbla bindningar mellan kol, medan fetter endast har enstaka bindningar mellan sig kol.
För att omvandla en olja till ett fett räcker det sålunda att hydrera oljan. På så sätt kommer dina dubbelbindningar att brytas om och konverteras till enstaka obligationer. Resultatet är produktion av samtal hydrerade vegetabiliska fetter.
- Alkyne-hydrering: Eftersom alkyner har två pi-bindningar sker deras fullständiga hydrering i två steg, i det första bildas en alken och i det andra en alkan.
I reaktionen nedan har vi hydreringen av propyn med slutlig bildning av propan:
Första steget: H3C C ≡ CH + H2 → H3C CH═ ÇH2
2: a etappen: H3C CH═ ÇH2 + 2 timmar2 → H3C CH2─ ÇH3
Om vi vill att denna reaktion ska upphöra i första steget måste vi använda något ämne som stoppar katalysatorns verkan.
- Hydrogenering av diener: Det finns tre typer av diener: ackumulerade (dubbelbindningar visas nedan), isolerat (dubbelbindningar är åtskilda av minst två enkelbindningar) och konjugat (dubbelbindningar visas omväxlande).
Hydreringen av ackumulerade och isolerade diener sker på samma sätt som vi såg för alkener, men i dubbelt, eftersom diener har mer omättnad. Se två exempel:
* Exempel på hydrering i ackumulerad dien:
H H H
│ │ │
H3C CH ═ Ç ═ CH ─ CH3 + 2 timmar2 → H3C CH ─ Ç ─ CH ─ CH3
│ │ │
H H H
* Exempel på hydrering i isolerad dien:
H H H H
│ │ │ │
H3C CH ═ CH─CH2 ─ CH ═ CH ─ CH3 +2 H2 → H3C CH ─ CH─CH2 ─ CH ─ CH ─ CH3
Å andra sidan kan hydreringen av konjugerade diener ske på två sätt: med 1,2 tillsats och 1,4 tillsats. Den vanligaste är 1,2-tillsatsen, där väten tillsätts till kol som ger dubbelbindning och vid låga temperaturer. 1,4-tillsatsen, å andra sidan, sker vid förhöjda temperaturer och är när det finns resonans och utseende av fria valenser i kol 1 och 4. Se exempel på varje fall:
* Exempel på 1,2 tillsats i konjugerade diener:
H2C CH ─ CH ═ CH2 + H2 → H2C CH ─ C ─ CH CH2
│ │
H H
* Exempel på tillsats 1,4 i konjugerade diener:
H2C CH ─ CH ═ CH2 + H2 → H2C CH ═ CH CH2
│ │
H H
- Hydrogenering av aromater: Pi-bindningarna i bensenringen bryts och väteatomerna tillsätts till kol som bildar dessa bindningar.
Denna typ av total hydrering visas nedan:

Total bensenhydreringsreaktion
- Cyclanhydrogenering: Bildning av en alkan sker.
Exempel: Hydrogenering av cyklopropan:
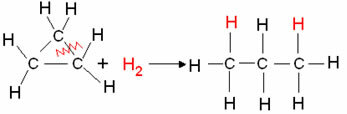
Cyklopropanhydreringsreaktion
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/reacao-organica-hidrogenacao.htm