händer med omvandlingisokorisk när en viss massa av en gas genomgår förändringar i temperatur som utlöser tryckförändringar eller tvärtom, med tanke på att temperatur och tryck, i detta fall, är direkt proportionella kvantiteter, medan systemvolymen förblir oförändrad.
Se också: Vad är partiellt tryck på gaser?
Vad är en isokorisk transformation?
En isokorisk omvandling är när en förändring i temperatur och tryck händer med en given massa gas, men dess volym förblir densamma. Tryckförändringen kommer att vara direkt proportionell mot temperaturen, det vill säga om en gas, i ett visst slutet system, fördubblar sin absoluta temperatur, kommer detta att orsaka en ökning av trycket till dubbelt så mycket som det ursprungligen var.
Denna typ av transformation kallas också isovolumetrisk eller isometrisk. Den isokoriska termen kommer från grekiska Isokhora, på vad iso betyder "lika" och khora betyder "plats eller volym" (i detta sammanhang).
Exempel:
En bils däck genomgår isokorisk omvandling, vi kan observera detta när vi gör det
kalibrering. På varma dagar är trycket på kalibreringsmonitorn högre än på kalla dagar. Detta beror på att med en ökning av temperaturen ökar trycket eftersom volymen förblir.
Andra exempel är spray deodoranter, i denna typ av produkt finns det en varning på etiketten som inte får förvaras eller utsättas för höga temperaturer, eftersom, förutom att några av dess ämnen är brandfarliga, finns det tillståndet för isokorisk transformation eller isovolumetrisk. Eftersom aerosoldeodoranterna är inne i en förseglad flaska och i gasformigt tillstånd en temperaturökning kommer att leda till en ökning av trycket och en explosionsrisk.
Kännetecken för en isokorisk transformation
- Konstant volym.
- Tryck och temperatur är direkt proportionella.
Dessa egenskaper kan beskrivas med följande formler:

Diagram över en isokorisk funktion
Observera följande tabell som beskriver en gas beteende i förhållande till tryck, temperatur och den resulterande konstanten.
Temperatur (° C) |
Tryck (atm) |
P / T = konstant |
50 |
5 |
10 |
100 |
10 |
10 |
150 |
15 |
10 |
200 |
20 |
10 |
Observera att trycket följer temperaturstegringen så att P / T-förhållandet förblir konstant, vilket innebär att tryck och temperatur är direkt proportionella. Därför är grafen som beskriver isokoriska transformationer av linjär typ. Se:

Vem upptäckte den isokoriska omvandlingen?
Jacques Alexandre César Charles (1746-1823) var den franska forskaren som studerade gasernas beteende i ett slutet system för att skapa en precisionstermometer och avslutade studierna om isokoriska transformationer.
Vetenskapsmannen Joseph Louis Gay-Lussac (1778-1850) utvecklade också en studie om expansion och krympning av ett gasformigt system. Dessa var oberoende analyser, men eftersom de kom till samma slutsats delade de poängen. Idag hänvisar vissa författare till de två sista fysiska lagarna om gaser som förklarar isobariska omvandlingar och isokorisk som 1: a och 2: a lagarna i Charles-Gay-Lussac.
Se också: Gay-Lussacs volymetriska lag
Övningarlöst
Fråga 1 - (PUC-RJ) Ett cykeldäck kalibreras med ett tryck på 4 atm, på en kall dag, vid en temperatur på 7 ° C. Volymen och mängden injicerad gas är densamma. Vad blir kalibreringstrycket i däcket när temperaturen når 37 ° C?
a) 21,1 atm
b) 4,4 atm
c) 0,9 atm
d) 760 mmHg
e) 2,2 atm
Upplösning
Alternativ A
Första steget: identifiera systemet och extrahera data.
Isovolumetriskt system
P1 = 4 atm
T1 = 7 ° C
T2 = 37 ° C
P2 =?
Med formeln:
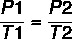
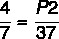
7 x P2 = 37 x 4
P2 = 148/7
P2 = 21,14 atm
Fråga 2 - (Unifor-CE) Undersök figuren nedan.
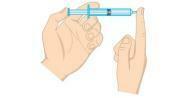
Gastrycket inuti sprutan kan minskas:
a) placera sprutan i isvatten och håll änden täckt.
b) att klämma ihop kolven och hålla änden täckt.
c) placera sprutan i varmt vatten och håll änden täckt.
d) öppna spetsen och driva ut halva luften ur sprutan.
e) dra i kolven och håll änden öppen.
Upplösning
Alternativ A. Trycket på en gas är direkt proportionellt mot temperaturen i ett isokoriskt system, det vill säga utan att ändra gasens volym eller massa. När temperaturen sjunker kommer trycket att sjunka.
Av Laysa Bernardes Marques de Araujo
Kemilärare
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/transformacao-isocorica.htm

