DE vinkelgeometri är en av flera typer av molekylär geometri, som fortfarande kan vara linjär, pyramidal, platt trigonal, tetrahedral, etc. Vinkelgeometri finns bara i molekyler som har följande egenskaper:
Triatomics, det vill säga de har bara tre atomer;
Ha minst tre elektronmoln i den centrala atomen.
Notera: elektroniskt moln är allt kovalent bindning (enkel, dubbel, trippel eller koordinat) mellan atomer och elektronpar av valenslager som inte deltar i ett samtal.
Se några exempel på molekyler som har vinkelgeometri:
1: a exemplet: vatten (H2O)

konventionell vattenstruktur
I vattenstrukturen har vi:
Tre atomer: två väten och ett syre;
Syre är den centrala atomen eftersom den skapar ett större antal bindningar (två, eftersom det tillhör VIA-familjen);
Två enkelbindningar mellan syre och väten. Detta beror på att varje väte bara kan skapa en bindning och syre två bindningar;
Fyra icke-bindande elektroner i syre, eftersom den har sex elektroner i valensskalet och endast använder två i bindningarna.
Som i vattenmolekylen finns det därför tre atomer och fyra elektroniska moln (två enkelbindningar och två icke-bindande elektronpar) i den centrala atomen, geometri är vinklad.
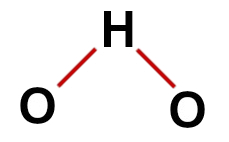
Rätt strukturformel för vatten
Notera: Närhelst molekylen presenterar dessa mönster är vinkeln mellan atomerna cirka 109º 28'.
2: a exempel: Svaveldioxid (SO2)

Konventionell struktur av svaveldioxid
I strukturen av svaveldioxid har vi:
Tre atomer: två oxygener och en svavelatom;
Svavel är den centrala atomen eftersom den är det minsta grundämnet i molekylen, eftersom alla element behöver göra samma antal bindningar (två);
En dubbelbindning mellan svavel och en av oxygenerna. Det beror på att båda behöver två anslutningar;
Ett koordinat eller dativ kovalent bindning, eftersom svavlet var stabilt efter parning med det andra syret, men det finns fortfarande en syreatom som behöver två elektroner;
Fyra icke-bindande elektroner i syre. Det beror på att syre har sex elektroner i valensskalet och endast använder två i bindningarna.
Såsom i svaveldioxidmolekylen finns det tre atomer och fyra elektroniska moln (två enkelbindningar och två par icke-bindande elektroner) i den centrala atomen, geometri är vinklad.
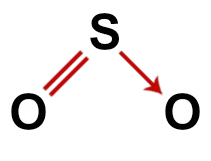
Korrekt strukturformel för svaveldioxid
Notera: Närhelst molekylen har dessa mönster är vinkeln som bildas mellan atomerna ungefär 120O.
Av mig Diogo Lopes Dias
Källa: Brazil School - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-geometria-angular.htm



