Ametaler är element som har en tendens att få elektroner och bilda anjoner (negativt laddade arter). Detta innebär att de släpps utelektronnegativitet, eller hög tendens att attrahera elektroner. Vi säger att ju mer elektronegativ en metall är, desto mer reaktiv blir den.
Experimentellt var det möjligt att bestämma ordningen på reaktiviteten för icke-metaller, vilket ges av följande:
F> O> N> Cℓ> Br> I> S> C> P> H
Se elektronegativitetsvärdena:
4,0 > 3,5 > 3,0 > 3,0 > 2,8 > 2,5 > 2,5 > 2,5 < 2,1
Det finns ett slags "trick" för att dekorera detta rad av elektronegativitet för icke-metaller, vilket ges av meningen nedan, där initialen för varje ord motsvarar symbolen för elementen i fråga:
“FHej Ohar inte NO Clube, brjag har ÄRAj Çdöende Pför Hsjukhus"
Men varför behöver vi känna till reaktiviteten hos icke-metaller? En anledning är att avgöra om den kemiska reaktionen kommer att äga rum eller inte.
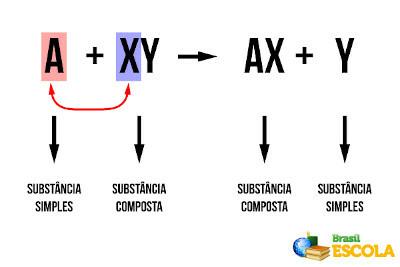
På enkla utbytes- eller förskjutningsreaktioner är de där en enkel substans (endast bildad av en typ av kemiskt grundämne) reagerar med a sammansatt substans och förskjuter ett av ämnena i ämnet och bildar ett nytt enkelt ämne och ett annat sammansatt. Generellt sett har vi:

Generisk förskjutningsreaktion
Se att "A" har skiftat "Y" och gått med i "X". Detta är också en redoxreaktion, eftersom det sker elektronöverföring. Med tanke på att "A" och "Y" är icke-metaller, har vi att "A" får elektroner (reducerad), bildar en anjon, och är en del av den sammansatta substansen "AX". Å andra sidan förlorade "Y", som var en anjon i den sammansatta substansen "XY", elektroner (den genomgick oxidation) och bildade den nya enkla substansen "Y".
När denna typ av reaktion inträffar är det nödvändigt att analysera reaktiviteten hos icke-metaller för att se om grundämnet av den enkla substansen kommer faktiskt att ha den reaktivitet som är nödvändig för att förskjuta det icke-metalliska från ämnet. sammansatt. Tänk till exempel på reaktionen mellan fluor och natriumklorid:
F2 (aq) + 2 NaCl(här) → ?
Gör fluor (F2) kan den förskjuta klor från natriumklorid (NaCl) och bilda en ny förening med natrium? I reaktivitetslinjen för icke-metaller är fluor mer reaktivt än klor. Så det lyckas förskjuta klor från NaCl, och reaktionen sker enligt följande:
F2 (aq) + 2 NaCl(här) → 2 NaF(här) + Cl2 (aq)
Eftersom det är mer elektronegativt har F2 (aq) reducerades och varje fluoratom fick en elektron och bildade anjonen F-(här). Denna anjon bildar en jonbindning med Na-katjonen.+(här)alstrar natriumfluorid (NaF). Under tiden, Cl anion-(här), som var en del av natriumklorid (NaCl), oxiderade och bildade kloratomer som förenade och bildade den enkla substansen Cl2.
Se nu ett annat exempel nedan. Kommer denna reaktion att ske?
Jag2 (aq) + KCl(här) → ?
Om vi tittar på reaktivitetskön för ametaler kommer vi att se det kommer inte att ske inga redoxreaktioner mellan dessa ämnen, eftersom Cl är mer reaktiv än jag, därför2 den kommer inte att ha den nödvändiga kraften för att förskjuta Cl från KCl-substansen.
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/ordem-reatividade-dos-ametais.htm