I många läkemedel och flytande och fasta livsmedelsprodukter, såsom vinäger och kex, t.ex. innehåll i procent massa av löst ämne (m1) i förhållande till massan av hela lösningen (m = m1 + m2). Denna storlek kallas Titel (T) eller massprocent av en lösning.
Dess definition kan uttryckas enligt följande:

Således görs dess beräkning genom den matematiska ekvationen nedan:
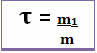
eller

Eftersom både nämnaren och täljaren har att göra med samma enhet (massenheten är gram - g) har titeln ingen enhet och är mindre än 1.
Således, om vi säger att titeln på en given lösning är 0,4, betyder det att för varje massaenhet i lösningen motsvarar 0,4 massan av lösningen. Emellertid uttrycks titeln ofta i procent. För att göra detta, multiplicera bara värdet med 100%. I det här fallet kallas det Massprocent (T%) *
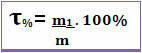
Notera figuren nedan, där viktprocenten natriumklorid i en saltlösning anges:

Saltlösning, som används vid behandling av uttorkning, innehåller en massprocent av natriumklorid på 0,9%
I det här fallet betyder det att för varje 100 g eller 100 enheter av denna lösning finns det 0,9 g eller 0,9% löst ämne, det vill säga natriumklorid (NaCl - bordssalt).
Ett annat exempel är ättika: på etiketten finns det en indikation på att 5% av massan ättiksyra användes i dess beredning, det vill säga det finns 5 g av denna syra för varje 100 g lösning.

Titeln kan också anges i volymprocent. I det här fallet är den enda skillnaden att istället för att relatera massan av löst ämne till massan av lösningen; volymen av det lösta ämnet är relaterat till volymen av lösningen, enligt följande formel:
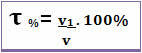
Till exempel, när det gäller vanlig alkohol, som har en volymprocent på 96%, i 100 ml lösning är 96 ml alkohol.

* Termen "titel" används mer bland forskare, medan tekniker och flera bokförfattare använder uttrycket "massprocent" oftare.
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/titulo-ou-porcentagem-massa.htm

