De bränslen som används i de flesta bilar är bensin och etanol. Den fullständiga förbränningen av dessa två bränslen genererar koldioxid (CO2 (g)) och vatten (H2O). Tyvärr kan emellertid ofullständig förbränning och föroreningar i alkohol och bensin generera ämnen som är mycket förorenande för miljön. När det gäller bensin, kolmonoxid (CO(g)); kolväten (föreningar som består av kol och väte), såsom etan (C2H6 (g)); och kväveoxider (NOx), huvudsakligen kvävemonoxid (NO) och kvävedioxid (NO2 (g)).
Således, för att undvika en ökning av luftföroreningar, behöver alla bilar anropad utrustning katalysator eller katalysator, som är en föroreningsskyddande anordning, som har till uppgift att behandla dessa gaser som frigörs av förbränningsmotorn och omvandla dem till mindre skadliga gaser. Katalysatorer används också för detta ändamål i vissa industriella processer.
De nämnda förorenande gaserna lämnar motorn och går in i katalysatorn och passerar genom ett slags "bikupa", vars celler i allmänhet är gjorda av keramiskt eller metalliskt material, som är belagt med aluminiumoxid (aluminiumoxid - Al
2O3). Denna bikakeform, med små kanaler, är viktig eftersom den ger en stor kontaktyta för gaserna, vilket gör att de reagerar snabbare.Men den verkliga katalysatorn är en metall som sitter ovanpå aluminiumoxid. Vanligtvis är de använda metallerna palladium, rodium, platina eller molybden. Du kan också blanda dessa metaller och använda legeringar. Till exempel, i fallet med bensin, används normalt en legering av palladium och torium; i fallet med etanol används en annan legering av palladium och molybden. Dessa metaller utför en heterogen katalys med förorenande gaser.
heterogen katalys det är en typ av reaktion där katalysatorn bildar ett flerfassystem med reaktanterna (i detta fall de förorenande gaserna). Detta beror på att katalysatorn adsorberar, det vill säga den behåller reaktantmolekylerna på dess yta, försvagar deras bindningar och gör att reaktionen fortgår snabbare.
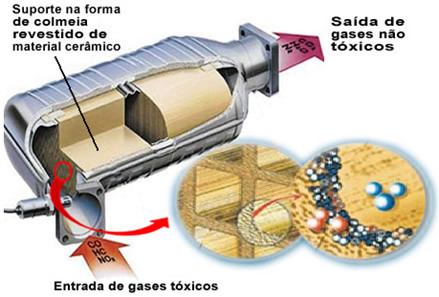
Som ett resultat omvandlar katalysatormetaller förorenande ämnen såsom CO och NOx i giftfria gaser som CO2, H2O, O2 och nej2. Se några av dessa reaktioner nedan och notera att genom dem sker oxidation av kolväten och CO (härledd från ofullständig förbränning) och även minskningen av kväveoxider till kvävgas (N2):
2 CO(g) + 2 NEJ(g) → 2 CO2 (g) + 1 N2 (g)
2 CO(g) + 1 O2 (g) → 2 CO2 (g)
2C2H6 (g) + 7 O2 (g) → 4 CO2 (g) + 6 H2O(v)
2 NEJ2 (g) +4 CO(g) → 1 N2 (g) + 4 CO2 (g)
2 NEJ2 (g) → 1 N2 (g) + 2 O2 (g)
2 NEJ(g) → 1 N2 (g) + 1 O2 (g)
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/conversor-catalitico.htm
