De oxidationsreduktionsreaktioner som huvudsakligen studerats i fysikalisk kemi är de där elektronöverföring sker. Den reagerande arten (atom, jon eller molekyl) som förlorar en eller flera elektroner är den som genomgår oxidation. Den kemiska arten som tar emot elektroner minskar däremot.
I allmänhet kallas det för denna typ av reaktion i oorganisk kemi enkel utbytesreaktion eller förskjutning.
För att någon reaktion ska äga rum är det nödvändigt att uppfylla vissa villkor. En av dem är att det måste finnas kemisk affinitet mellan reagenserna, det vill säga de måste interagera på ett sådant sätt att de möjliggör bildandet av nya ämnen.
När det gäller redoxreaktioner betyder affinitet att en av reaktanterna tenderar att få elektroner och den andra tenderar att förlora elektroner. Denna trend motsvarar reaktivitet av de involverade kemiska elementen.
Låt oss se hur det är möjligt att jämföra reaktiviteten mellan metaller.
Antag att vi vill lagra en lösning av koppar II-sulfat (CuSO4). Vi kunde omöjligt placera den här lösningen i en aluminiumbehållare, eftersom följande reaktion skulle inträffa:
2 Al(s) + 3 CuSO4 (aq)→ 3 Cu(s) + Al2(ENDAST4)3 (aq)
Observera att aluminium har oxiderat, förlorat 3 elektroner vardera och blivit aluminiumkatjon:
Al(s) → Al3+(här) + 3 och-
Samtidigt koppar katjonen (Cu2+) som var närvarande i lösningen fick elektroner från aluminium och reducerades och blev metallisk koppar. Varje kopparkatjon tar emot två elektroner:
Röv2+(här) + 2 och- → Cu(s)
Men om det var tvärtom och vi ville lagra en lösning av aluminiumsulfat (Al2(ENDAST4)3 (aq)), skulle det inte vara ett problem att placera den i en kopparbehållare, eftersom denna reaktion inte skulle inträffa:
Röv(s) + Al2(ENDAST4)3 (aq) → händer inte
Dessa observerade fakta kan förklaras av det faktum att aluminium är mer reaktivt än koppar.
Metaller har en tendens att ge upp elektroner, det vill säga att oxidera. När man jämför olika metaller, den som har den största tendensen att donera elektroner är den mest reaktiva. Följaktligen är metallernas reaktivitet också associerad med deras joniseringsenergi, det vill säga den minsta energi som behövs för att avlägsna en elektron från den gasformiga atomen i dess jordtillstånd.

Baserat på detta, metallreaktivitetskö eller rad elektrolytiska spänningar, visas nedan:
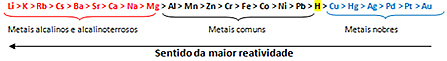
Den mest reaktiva metallen reagerar med joniska ämnen vars katjoner är mindre reaktiva. Med andra ord reagerar metallen till vänster med det ämne som bildas av joner till höger. Motsatsen händer inte.
Kom ihåg exemplet som ges, se i reaktivitetsraden att aluminium (Al) är till vänster om koppar (Cu). Därför reagerar aluminium med den lösning som bildas av kopparkatjoner; men koppar reagerar inte med en lösning bildad av aluminiumkatjoner.
Observera att den mest reaktiva metallen är litium (Li) och den minst reaktiva är guld (Au).

Detta är en av anledningarna till att guld är så värdefullt, för om det inte reagerar förblir det intakt under lång tid. Detta kan ses i de guldbelagda egyptiska sarkofagerna och skulpturer som går tillbaka till den mest avlägsna antiken. Vi visualiserar också detta när vi jämför hållbarheten hos ett rent guldsmycke med smycken tillverkade av andra metaller som är mer reaktiva än guld.

Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/ordem-reatividade-dos-metais.htm
