Forskaren Friedrich Kohlrausch (1840-1910) var den första som föreslog att rent vatten leder elektricitet, om än i liten skala. Detta beror på att vatten beter sig på ett amfotärt sätt; det vill säga vid vissa tillfällen fungerar det som syra som donerar protoner (H+); och i andra beter sig det som en bas och tar emot protoner.
Detta innebär att vatten utför sin egen jonisering enligt den kemiska ekvationen som visas nedan:
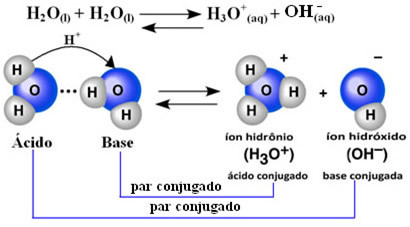
Denna process kallas vatten autojonisering och det förekommer i mycket liten skala, det vill säga vatten är en mycket svag elektrolyt, med låga värden av joniseringsgrad och joniseringskonstant vid jämvikt (Kç). Det är just därför vatten har så låg konduktivitet.
För att få en uppfattning är det vid en omgivningstemperatur på 25 ° C möjligt att bestämma att koncentrationerna av hydroxid och hydroniumjoner som produceras vid självjoniseringen av rent vatten är lika med 1. 10-7 mol. L-1. Det betyder att av två miljarder vattenmolekyler bara två joniseras.
Den joniska balanskonstanten för vatten kallas
çvattendissociationskonstant,autoprotolys konstanteller jonisk produkt av vatten.Denna konstant representeras av Kw, eftersom w hänvisar till ordet vatten, som på engelska betyder vatten.Dess beräkning görs på samma sätt som de andra jämviktskonstanterna, kom ihåg att, som anges i texten "Konstanter av Balansera Kc och Kp ”, i detta fall visas endast produkterna i uttrycket, eftersom vatten i flytande tillstånd har samma aktivitet till 1. Rena flytande eller fasta ämnen läggs inte i uttrycket för dissociationskonstanten eftersom de inte förändras. Endast vattenhaltiga och gasformiga lösningar placeras. Så vi har:
Kw = [H3O+]. [åh-]
Kw = (1. 10-7). (1. 10-7)
Kw = 10-14
Som med de andra jämviktskonstanterna, OKw det ändras bara med temperaturförändringen. När vattentemperaturen ökar ökar dess jonisering också, vilket innebär att självjoniseringen av vatten är en endoterm process, det vill säga det absorberar värme.
Detta kan ses i värdena för den joniska produkten av vatten (Kw) i tabellen nedan vid olika temperaturer:
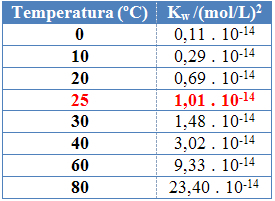
Den joniska produkten av vatten kommer alltid att ha ett fast värde vid varje temperatur, antingen i rent vatten eller i lösning. Även om lösningen har koncentrationer av H-joner3O+ och åh- annorlunda förblir produkten mellan dem konstant.
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/produto-ionico-Agua-kw.htm
