DE Organisk kemi är en del av kemi som varje år har fått framträdande i antagningsprov och i Enem, särskilt ämnet organiska reaktioner. Med det i åtanke nedan kommer du att ha tillgång till grundläggande tips om organiska reaktioner för att underlätta dina studier!
1) Hur man känner igen en förbränning
Förbränningsreaktion är en där någon organisk förening (såsom metan) reagerar med syrgas för att bilda vatten och en koldioxid (såsom koldioxid).
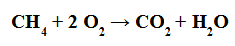
Ekvation som representerar förbränningen av en organisk förening
2: a) Vilka produkter har sitt ursprung i en förbränningsreaktion?
Produkterna som har sitt ursprung i en förbränningsreaktion beror på typen av förbränning:
Komplett förbränning: är den där vi har bildat vatten och koldioxid (CO2) .
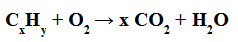
Exempel på en fullständig förbränningsekvation
Ofullständig förbränning: är den där vi bildar vatten och kolmonoxid (CO).

Exempel på ofullständig förbränningsekvation
3: a) Vilka ämnen är inblandade i en reaktion av fotosyntes?
Fotosyntesreaktionen inträffar när koldioxidmolekyler reagerar med vattenmolekyler, i närvaro av ljus och klorofyll, för att bilda kolhydratmolekyler (såsom glukos).
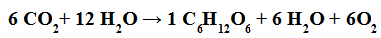
Kemisk ekvation som representerar fotosyntes
Tilläggsreaktioner är de där pi-bindningarna i en kedja bryts, och var och en av kol som gjorde dessa bindningar får nya atomer.
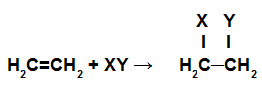
Schematisk framställning av en tilläggsreaktion
5.) Vilka är de möjliga reaktanterna för en tillsatsreaktion?
Organiska ämnen som vanligtvis används i en tillsatsreaktion är:
alken: Organisk substans bildas endast av kol och väten, i en öppen kedja med en dubbelbindning.
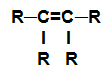
Strukturformel för en alken
OBS: R-gruppen kan vara en radikal eller ett väteelement.
alkyn: Organisk substans bildas endast av kol och väten, i en öppen kedja med en trippelbindning.
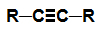
Strukturformel för en alkyn
alkadien: Organisk substans bildas endast av kol och väten, i en öppen kedja med två dubbelbindningar.
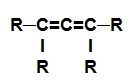
Strukturformel för en alkadien
Cyclan:Organisk substans bildas endast av kol och väten, i en sluten och mättad kedja.
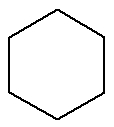
Strukturformel för en cyklan
Cyklonisk: Organisk substans bildas endast av kol och väten, i en sluten och mättad kedja.
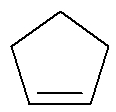
Strukturformel för en cyklene
Bensen
Organisk substans bildad av en sluten kedja och består av sex kolatomer, tre alternerande dubbelbindningar och sex väteatomer.

Strukturformel av bensen
6: e) Vilka är de möjliga produkterna från en tillsatsreaktion?
Produkterna från en tillsatsreaktion beror på ämnet som reagerar med de organiska föreningarna (alken, alkyn, alkadien, etc.). Se de viktigaste tilläggsreaktionerna och deras möjliga produkter:
Dessa är reaktioner där, förutom den organiska substansen, en av reaktanterna måste vara vätgas (H2). I denna reaktion bryts pi-bindningen och var och en av kol som bildade bindningen får en väteatom. Om det finns mer än en pi-länk upprepas processen. Det bildas ett kolväte.
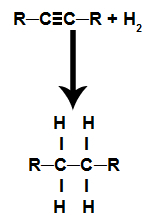
Ekvation som representerar hydreringen av en alkyn
Dessa är reaktioner där, förutom den organiska substansen, en av reaktanterna måste vara en enkel substans bildad av halogen. I denna reaktion bryts pi-bindningen och var och en av kol som gjorde bindningen får en halogenatom. Om det finns mer än ett pi upprepas processen.
Vi kommer att bilda organiska halider vicinals (de där två kol i kedjan är grannar och innehåller halogen).
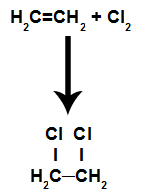
Ekvation som representerar kloreringen av en alken
c) Tillsats med syrahalogenid
Dessa är reaktioner där, förutom den organiska substansen, ett av reagensen måste vara en syrahalogenid (HCl, HBr, HI, HCl). I denna reaktion bryts pi-bindningen och väte i syran går till ett kol och halogen går till ett annat. Om det finns mer än ett pi upprepas processen. Vi kommer att bilda ett kolväte.
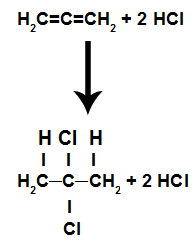
Ekvation som representerar syrahalogenidadditionen av en alkadien
d) Hydrering
Dessa är reaktioner där, förutom den organiska substansen, en av reaktanterna måste vara vatten (H2O). I denna reaktion bryts pi-bindningen och väte i vatten går till ett kol och OH-gruppen i vatten går till ett annat kol. Om det finns mer än ett pi upprepas processen. Vi kommer att bilda ett kolväte.
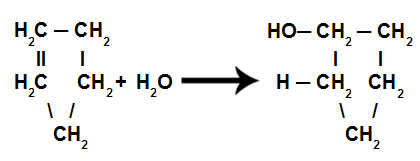
Ekvation som representerar cyklens hydrering
7: e) Hur man känner igen en substitutionsreaktion
En substitutionsreaktion är en där en organisk förening byter ut en eller flera väteatomer med en atom eller grupp av substansen som reagerar med den.

Schematisk framställning av en substitutionsreaktion
8.) Vilka är de möjliga reaktanterna för en substitutionsreaktion?
De organiska substanserna som vanligtvis används i en substitutionsreaktion är:
alkan: Organisk substans bildas endast av kol och väten, i en öppen och mättad kedja.
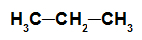
Strukturformel för en alkan
Bensen
Redan demonstrerat i 5: e tipset.
→ Bensenderivat: organiska ämnen i vilka ett eller flera väten byts mot andra atomer eller olika grupper.
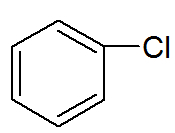
Strukturformel för ett bensenderivat
organisk halogenid
Organisk substans bildad av atomer av kol, väte och en eller flera halogener (klor, brom, jod och fluor), i en öppen eller sluten kedja, mättad eller omättad.

Strukturformel för en organisk halogenid
9) Vilka är de möjliga produkterna från en substitutionsreaktion
Produkterna från en substitutionsreaktion beror på ämnet som reagerar med de organiska föreningarna. Se de viktigaste ersättningsreaktionerna och deras möjliga produkter:
a) Halogenering
Detta är reaktioner där, förutom den organiska substansen, en av reaktanterna måste vara en enkel substans bildad av halogen.
I denna reaktion ersätts ett väte i den organiska föreningen med en halogenatom som bildar en syrahalogenid och en oorganisk syra.

Ekvation som representerar kloreringen av en alkan
Reaktion där den organiska föreningen reagerar med salpetersyra (HNO3). I denna reaktion förlorar föreningen väte och tar emot nitrogruppen (NO2), vilket resulterar i en nitroförening och vatten, oavsett vilken organisk förening som har reagerat med syran.
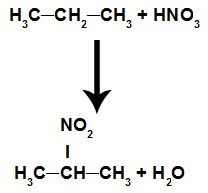
Ekvation som representerar alkanitrering
Reaktion vid vilken den organiska föreningen reagerar med svavelsyra (H.2ENDAST4). I denna reaktion förlorar föreningen ett väte och tar emot sulfongruppen (SO3H), vilket resulterar i a sulfonsyra och vatten, oavsett vilken organisk förening som har reagerat med syran.

Ekvation som representerar bensensulfonering
Reaktion där den organiska föreningen reagerar med en organisk halogenid. I denna reaktion förlorar den organiska föreningen ett väte och tar emot den radikal som fästes till halogenen i den organiska haliden. Reaktionen resulterar i kolväte och en oorganisk syra, oavsett vilken organisk förening som har reagerat med syran.

Ekvation som representerar alkyleringen av bensen
Reaktion där den organiska föreningen reagerar med a syrahalogenid.
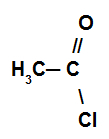
Exempel på en syrahalogenid
I denna reaktion förlorar den organiska föreningen ett väte och tar emot acylgruppen från syrahaliden.
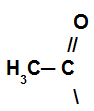
Representation av acylgruppen i syrahalogeniden
Reaktionen resulterar i en keton och en oorganisk syra, oavsett vilken organisk förening som har reagerat med syran.
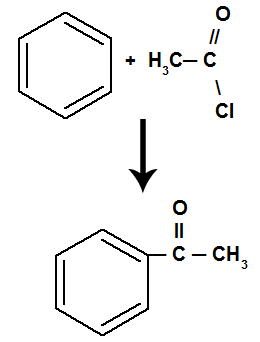
Ekvation som representerar acylering av bensen
Av mig Diogo Lopes Dias
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/dicas-fundamentais-sobre-reacoes-organicas.htm
