O atomstråle av element är en periodisk egenskap som bestämmer en atoms radie som varierar beroende på elementets position i det periodiska systemet.
Således kan de öka och minska som atomnummer (Z) av elementet som motsvarar antalet protoner som finns i atomkärnan.
Sammanfattningsvis motsvarar atomradien halva avståndet mellan kärnorna i två angränsande atomer, uttryckt enligt följande:
r = d / 2
Varav:
r = radie
d = kärnavstånd
I allmänhet mäts atomradien i pikometrar (pm), delmultipel av mätaren (1 pikometer = 10-12 m.). Observera att när referensen inte är en atom utan en jon är radien som hittats den joniska radien.
Atomic Radius Variation
I det periodiska systemet kan atomradiens tillväxt ses i följande figur:
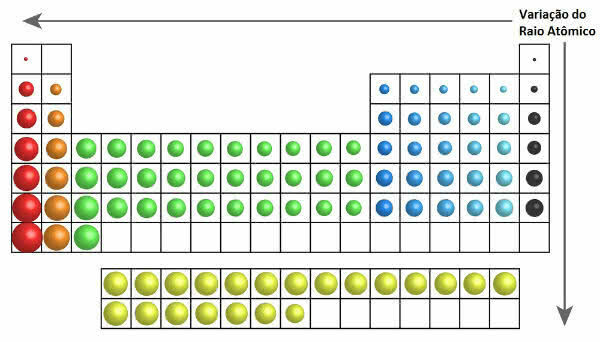 Atomic Radius Variation in the Periodic Table
Atomic Radius Variation in the Periodic Table
Således ökar atomradien vertikalt (familjer eller grupper) från topp till botten. På det horisontella (perioderna) ökar de från höger till vänster.
Se den omvända variationen i Elektronisk tillhörighet och elektronnegativitet.
Joniseringsenergi
DE joniseringsenergi (eller potential) det är också en periodisk egenskap som bestämmer den energi som krävs för att skifta en elektron, som uttrycks i elektronvolt (eV).
Läs också: Periodiska egenskaper.
Kolla frågor om inträdesprov med en kommenterad resolution i: Övningar på det periodiska systemet.