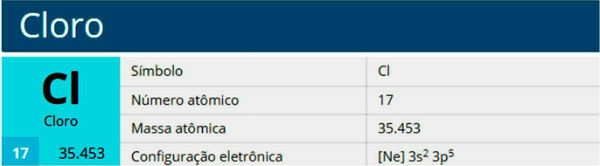
Klor är ett kemiskt grundämne med symbolen Cl, atomnummer 17, atommassa 35,5. Den tillhör halogenfamiljen, grupp 17 eller 7A, och till den tredje perioden i det periodiska systemet.
Dess namn kommer från grekiska khloros, vilket betyder grönaktigt. Detta beror på att klor under normala temperatur- och tryckförhållanden kännetecknas av att det är en gröngul gas med stark lukt.
Funktioner
Klor upptäcktes 1774 av den svenska forskaren Carl Wilhelm Scheele (1742-1786). Men vid den tiden trodde jag att det var en förening med syre. År 1810 demonstrerade Humphry Davy (1778-1829) att det var ett nytt kemiskt grundämne.
Eftersom det är ett extremt reaktivt element, finns det knappast i naturen i sin rena form, med undantag för den lilla mängd som släpps ut under vulkanutbrott i form av HCl.
Således finns det vanligtvis i form av natriumklorid (NaCl), även känd som bordssalt. I mineraler förekommer det i form av karnallit och sylvit.
Det kan också erhållas med elektrolys NaCl i vattenlösning. Klor producerar också många salter från klorider genom processen för oxidation.
Läs mer, läs även:
- Periodiska systemet
- Kemiska element
- Halogener
applikationer
Klorgas (Cl2) är giftigt och irriterande, detta tillstånd ledde till att det användes som ett kemiskt vapen under första världskriget. Denna gas orsakar irritation i luftvägarna och huden, vattenretention i lungorna, sönderrivning och vid inandning i stora mängder kan leda till döden.
Några andra användningar av klor är:
- Blekning av papper och tyger med klordioxid (ClO2).
- Vattenbehandling, tillsats av klor gör vattnet drickbart och lämpligt för konsumtion. Denna process kallas klorering och använder hypoklorsyra (HClO).
- Desinfektion av poolvatten och industriavfall, eftersom klor kan döda mikroorganismer.
- Tillverkning av plastföreningar som PVC (polyvinylklorid) och syntetiskt gummi.
- Produktion av vissa typer av organiska och oorganiska föreningar.