Du oxider de består av två olika element, varav ett är syre, som måste vara det mest elektronegativa av de två.
Nomenklaturen för oorganiska oxider följer regler som beror på om oxiden är molekylär, kovalent eller jonisk. Låt oss titta på varje fall:
* Nomenklatur för molekylära oxider eller kovalent nätverk:
Molekylära eller kovalenta nätverksoxider är de som har syre fäst vid a ametalsåsom kol (C), kväve (N), svavel (S), fluor (F), bland andra. Nomenklaturen för dessa oxider följer följande regel:

Nomenklaturregel för oxider bildade med icke-metaller
Monoprefixet framför det syrlänkade elementet är valfritt.
Till exempel har vi följande molekylära oxid: CO.
- Prefix som anger mängden syre: 1 syre: mono;
- oxid av;
- Prefix som anger antalet atomer för det andra elementet: 1 kol: mono;
- Namnet på det element som är kopplat till syre: kol.
Så ditt namn är så här: CO = monokolmonoxid eller kolmonoxid.
Se fler exempel:
koldioxid - CO2
Svaveltrioxid - SO3
Diklorheptoxid - Cl2O7
Dinitrogen Monoxide - N2O
Dinitrogen trioxide - N
Kvävemonoxid -NO
Kvävedioxid - NEJ2
Dinitrogen pentoxide - N2O5
Kiseldioxid - SiO2
Difosforpentoxid - P2O5
Svaveltrioxid - SO3
* Nomenklatur för jonoxider:
Jonoxider är de som har syre bundet till a metallsåsom järn (Fe), bly (Pb), natrium (Na), kalcium (Ca), silver (Ag), bland andra. Generellt är den elektriska laddningen av syre -2.
Nomenklaturen som nämns för molekylära eller kovalenta nätverksoxider tillämpas för närvarande även på metalloxider och anses vara officiell. Se några exempel:
Järnmonoxid - FeO
Blymonoxid - PbO
Blydioxid - PbO2
Diferös trioxid - Fe2O3
Det finns dock en specifik nomenklatur för metalloxider som fortfarande används i stor utsträckning. Den är baserad på valensen av det element som är kopplat till syre.
Om elementet har en enda valens, det vill säga om det bara finns ett sätt att binda syre och endast bilda en typ av oxid, kommer namngivningsregeln att ges av:

Regler för namngivning av jonoxid med en enda valent
Exempel:
- Natriumoxid - Na2O
- Kalciumoxid - CaO
- Kaliumoxid - K2O
- Aluminiumoxid - Al2O3
- Silveroxid - Ag2O
Men det finns också jonoxider bildade av element med mer än en valens. I dessa fall är namngivningsregeln följande:
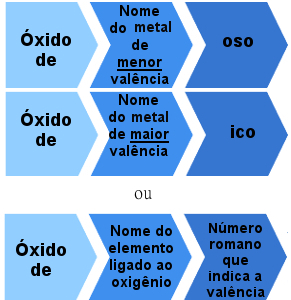
Nomenklaturregel för jonoxider med mer än en valens
Exempel:
Järnoxid - FeO
Järnoxid - Fe2O3
Cuprous Oxide - Cu2O
kopparoxid - CuO
Eller:
Järnoxid II - FeO (Järn nox = +2)
Järnoxid III - Fe2O3 (Järn nox = +3).
Kopparoxid I - Cu2O (Järn nox = +1)
Kopparoxid II - CuO (Järn nox = +2).
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/nomenclatura-dos-oxidos.htm
