Har du någonsin provat att tvätta bara med vatten?─ Det fungerar inte, eller hur ?!Varför kan inte vatten ensam ta bort fett och smuts?Det där det händer eftersom sammansättningen av dessa material skiljer sig väldigt mycket från sammansättningen av vatten, vilket gör det svårt för dem att blanda.
Vi säger att vattenmolekyler är det polärdet vill säga de har delar som är laddade: en del är positiv och den andra är negativ.Fetter och oljor är apolar, vilket innebär att dess molekyler inte har någon laddning.Således kan de polära vattenmolekylerna inte tränga igenom fettmolekylerna och dra dem med. Det är av samma anledning som olja inte blandas med vatten, som visas i följande bild:

Vatten och olja blandas inte eftersom vatten är polärt och olja är opolärt
Ett annat problem är att vattenmolekylerna bildar ett slags "hud" eller "film" som gör det ännu svårare för det att tränga igenom smutsen. Detta tunna skikt kallas vattenspänning. Dess bildning inträffar eftersom den positiva delen av en vattenmolekyl drar till sig den negativa delen av en annan vattenmolekyl, och så vidare.
På detta sätt är molekylerna mycket nära varandra, särskilt ytmolekylerna och bildar filmen vi pratade om. Följande illustration visar hur vattenmolekyler (symboliserade med de blå kulorna) lockar varandra och skapar ytspänning:
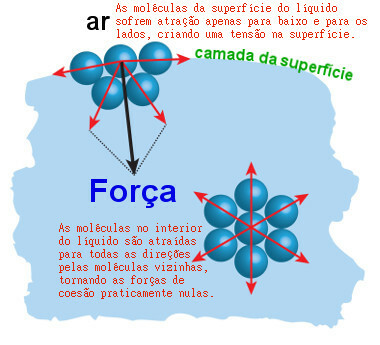
Ytspänning är en "film" bildad av attraktionskrafterna mellan ytvattenmolekyler
Bevis på att vatten faktiskt har denna "film" visas i bilden nedan, där en insekt kan gå ovanpå vatten:

Insekt på vatten på grund av intensiv ytspänning
Så för att kunna rengöra fett och smuts måste vi använda tvål.Men hur fungerar tvål? Hur rengör den?
I grund och botten, tvålen lyckas "bryta" denna "film" av vatten, så att den kan tränga in i materialen och ta bort smutsen. Det är därför tvål ofta kallas a tensid eller tensid, För att han minskar vattens ytspänning. Det är som om tvålen gjorde vattnet "våtare", vet du ?!
Men hur får han det?För att förstå, titta på bilden nedan som visar strukturen på en tvål:
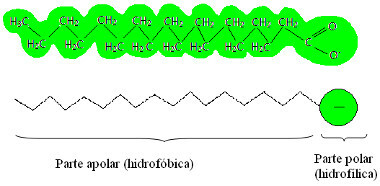
Typisk struktur för en tvål
Se till att tvålen har en del som är opolär (liksom fett och olja)och en annan del som är polär (precis som vatten).På detta sätt interagerar den icke-polära delen av tvålmolekylen med de icke-polära molekylerna av fetter och oljor,och den polära delen interagerar med de polära molekylerna i vatten.
Tvålmolekyler fördelar sig och bildar miceller, som följande bild visar:
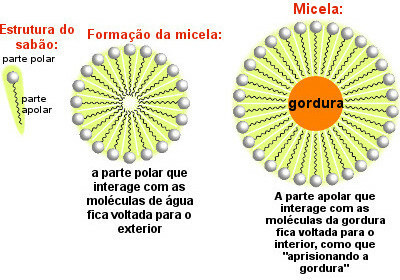
Tvål Mixen inslagningsfett
Observera att den icke-polära delen av tvålmolekylerna omger fettpartikeln som dras med av vattnet som är i kontakt med tvålens polära del utåt. Således hjälper micellerna som bildas av tvålen att avlägsna den fettiga smutsen.
Av Jennifer Fogaça
Examen i kemi



