Batteri är en anordning där en elektrisk ström produceras från kemisk energi som kommer från a oxidoreduktionsreaktion, det vill säga en art av reaktanten förlorar elektroner (oxidation), medan en annan art får elektroner (reduktion).
Se representationer av oxidations- och reduktionsreaktionerna som uppstår i vilken stapel som helst:
Oxidation: X → och + X+
Art X tappar en elektron och förvandlas till en katjon.
Minskning: Y- + och → Y
Y-anjonen- får elektron och förvandlas till en neutral Y-art.
Grundläggande komponenter i en stack
De grundläggande komponenterna i en stack är:
Anod: negativ elektrod i vilken oxidationsreaktionen äger rum, det vill säga förlust av elektroner;
Katod: positiv elektrod i vilken reduktionsreaktionen äger rum, det vill säga elektronförstärkning;
Elektrolytisk lösning (saltbrygga) eller ett ledande material (såsom en grafitstång): är det sätt på vilket elektroner som ges av anoden når katoden.
Grunderna för hur ett batteri fungerar
Funktionen för en stack uppstår från följande händelser:
Första principen: Anodoxidation
Metallen i anoden, eftersom den har en större tendens att förlora elektroner, blir en katjon, som vi observerade i ekvationen nedan:
Zn → Zn2+ + 2 och
2: a princip: katodreduktion
Katjonerna som ingår i materialet som finns i katoden (vi kommer att använda koppar som ett exempel) vid mottagning elektronerna från anoden omvandlas till metallisk koppar, som vi kan se i ekvationen vrål:
Röv2+ + 2e → Cu
första högar
a) Alessandro Voltas batteri
Alessandros stapelbaksida (den första högen i historien), monterad 1800, bildades av interkalerade metallskivor, som i bilden nedan:

Montering som liknar Alessandros tillbaka till din hög
Skivorna sammanflätades eftersom de hade olika sammansättning. Den ena var gjord av zinkmetall och den andra gjordes av koppar, som alltid separerades med bomull blötläggd i saltlösning (en lösning bildad av vatten och salt).
B) Daniels hög
Daniels hög, monterad 1836, bestod av två halvceller förbundna med en ledningstråd och en saltbro.
Halvcell 1: det var anoden, det vill säga batteriets negativa pol.
Den bestod av en zinkplatta och en del av denna platta nedsänktes i en lösning bildad av vatten och zinksulfat (ZnSO4).
Halv cell 2: det var katoden, det vill säga batteriets positiva pol.
Den bestod av en kopparplatta, och en del av denna platta nedsänktes i en lösning bildad av vatten och kopparsulfat (CuSO4).
saltbro
U-format rör som innehöll en lösning bildad av vatten och kaliumklorid (KCl), som förbinder de två halvcellerna (zink och koppar) och hade en glasull i båda ändar.
batterier för närvarande
För närvarande finns det flera modeller av stackar, men i allmänhet ser de ut så här:
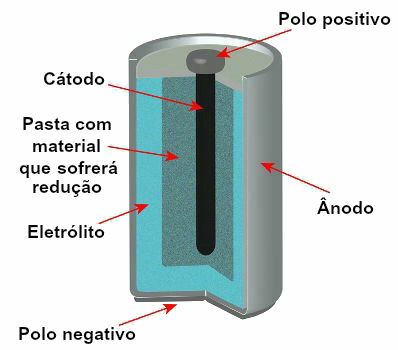
Schematisk bild av modellen för en aktuell stack
De mest använda modellerna är det så kallade Leclanché-batteriet och det alkaliska batteriet, som har följande skillnader:
De) Leclanche hög
Den har en anod bildad av metalliskt zink;
Den har en katod bildad av en pasta med ammoniumklorid, vatten, stärkelse och mangandioxid;
Den har en grafitstång som fungerar som ledare för elektronerna som avgår från katoden mot anoden.
B) Alkaliskt batteri
Den har en anod bildad av metalliskt zink eller kadmium;
Den har en katod bildad av kvicksilveroxid, nickeloxid och jod;
Den måste ha en blandad bas i materialet som utgör katoden.
Av mig Diogo Lopes Dias
Källa: Brazil School - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-pilha.htm
