Som anges i texten "Alfaemission (α)”, Nya Zeelands kemist Ernest Rutherford utförde ett experiment där han placerade ett prov av ett radioaktivt material i ett blyblock med ett hål för att styra de radioaktiva utsläppen; och utsatte dessa strålningar för ett elektromagnetiskt fält.
Bland de erhållna resultaten märkte Rutherford att en strålningsstråle lockades av den positiva plattan, vilket ledde honom till slutsatsen att dessa utsläpp var av negativ laddning. Denna strålning kallades strålareller beta-utsläpp (β).
Eftersom strålar drabbades när de utsattes för ett elektromagnetiskt fält ledde detta honom också till slutsatsen att de faktiskt var sammansatta av partiklar som har massa. Massan av dessa partiklar var dock mindre än partiklarna som utgjorde alfa-utsläppen, eftersom β-partiklarna fick större avvikelse.
- Konstitution:
År 1900 jämförde den franska fysikern Antoine-Henri Bequerel (1852-1908) dessa avvikelser som betapartiklar med de förskjutningar som elektroner utförde när de också utsattes för ett fält elektromagnetisk. Resultatet var att de var desamma; med det sågs det
betapartiklarna var faktiskt elektroner.Som ett resultat ges representationen av denna partikel av 0-1β eller β-. Observera att betaemissionen har ett massnummer (A) som är lika med noll, eftersom elektronerna inte är en del av atomens kärna.
- Konsekvenser av utsläpp av betapartiklar för atomens struktur:
Utsläpp av en beta-partikel (0-1β) är resultatet av omläggning av den instabila kärnan i den radioaktiva atomen för att få stabilitet. Därför inträffar ett fenomen i kärnan, där en neutron sönderdelas och härrör från tre nya partiklar: en proton, en elektron (partikel β) och en neutrino. Antineutrino och elektron släpps ut; protonen förblir dock i kärnan.
10Nej →11p + 0-1och + 00ν
neutron protonelektronneutrino
Således, när en atom avger en beta-partikel, ändras den till ett nytt element med samma massnummer (eftersom neutron som fanns tidigare "ersattes" av protonen), men dess atomnummer (Z = protoner i kärnan) ökar med en enhet.
Se nedan hur detta händer i allmänhet:
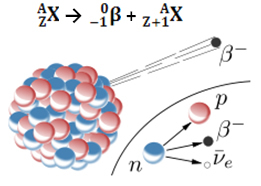
Här är ett exempel på betaförfall som inträffar med isotop 14 av grundämnet kol:

Betastrålning består av elektroner som sänds ut med hög hastighet av kärnorna i radioaktiva atomer, denna initialhastighet är från 100 000 km / s upp till 290 000 km / s och når 95% av hastigheten på ljus.
Massan av β-strålning är densamma som för en elektron, som är 1840 gånger mindre än för en proton eller neutron. Alfa (α) strålning avger två protoner och två neutroner, så massan av α-partiklar är 7360 gånger den för β-partiklar. Detta förklarar det faktum att α-partiklar lider av mindre avvikelse än β-partiklar, som Rutherford hade verifierat i sitt experiment.
- Penetrationskraft:
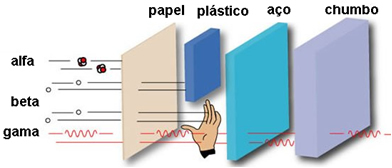
Dess penetrationsförmåga är medium och är 50 till 100 gånger mer penetrerande än alfapartiklar. Dessa kan passera genom ett pappersark men hålls av ett ark av endast 2 mm bly eller 2 cm aluminium. När de påverkar människokroppen kan de tränga upp till 2 cm.
- Skador på människor:
Eftersom dess penetrationsförmåga över människokroppen endast är 2 cm kan β-partiklarna tränga in i huden och orsaka brännskador, men stoppas innan de når organens mest inre organ i kroppen.
Av Jennifer Fogaça
Examen i kemi


