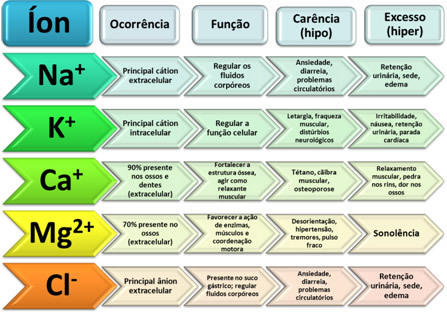
Dispersioner avser blandningar i allmänhet. När vi till exempel blandar salt med vatten eller salt och sand får vi två dispersioner. Ett ämne som sprids homogent (som salt i vatten) eller heterogent (som sand i vatten) kallas "spridd". Vatten, å andra sidan, fungerar som ett dispergeringsmedel i dessa fall.
Huvudskillnaden mellan dessa två dispersioner är i dispersionspartikelstorleken. Medan sandkornen kan ses med blotta ögat är saltpartiklarna osynliga. Baserat på detta kan dispersioner klassificeras i tre huvudtyper, vilka är:
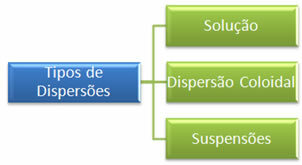
Observera, i tabellen nedan, skillnaden i storleken på de dispergerade partiklarna:

* Lösningar: de är homogena blandningar där vi inte kan se de dispergerade partiklarna ens under ett mikroskop. Några exempel är ovan nämnda salt blandat med vatten och även socker blandat med vatten.
I fallet med lösningar kallas dispersionen ett löst ämne och dispergeringsmedlet kallas ett lösningsmedel. Lösningar kan inte separeras med någon filtreringsprocess.
* Kolloidal eller kolloid spridning:
några exempel är majonnäs och gelatin. Dess partiklar visualiseras inte med blotta ögat, så de förväxlas ofta med homogena system, men de är faktiskt heterogena, vilket kan ses med användning av mikroskop. Dess partiklar avgör inte med gravitationens verkan, utan bara med ultracentrifuger.Sluta inte nu... Det finns mer efter reklam;)
Det finns flera typer av kolloidala dispersioner, vilka är: sol, fast sol, gel, emulsion, skum och aerosol.
Att separera denna typ av dispersion är inte möjligt med filtrering utan med ett halvgenomträngligt membran. Dess partiklar reflekterar och sprider ljus.
* Upphängningar: de är heterogena system, där det, även med blotta ögat, är möjligt att visualisera deras partiklar. Några exempel är: sand i vatten, lera i vatten, magnesia-mjölk och kalamin.
Vid spridning reflekteras också ljus. Och dess separering kan göras genom gemensam filtrering.

* Även om vissa författare och forskare har föreslagit att kolloidala partiklar har en storlek mellan 1 och 100 nm och att suspensioner är mer än 100 nm, tenderar experimentellt bevis att öka detta värde till 1000 nm, och detta värde är det mest accepterade av de flesta författare. Emellertid kommer dess makroskopiska beteende verkligen att avgöra om blandningen är kolloidal eller en suspension.
Av Jennifer Fogaça
Examen i kemi
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
FOGAÇA, Jennifer Rocha Vargas. "Typer av dispersioner"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/quimica/tipos-dispersoes.htm. Åtkomst den 28 juni 2021.