ТХЕ клапеирон једначина је математички израз који повезује величине као што су притиска (П), запремина (В), температура (Т) и број честица (н) које чине а савршен или идеалан гас. Ова једначина је добила име по француском физичару Паулемилеклапејрон и може се разумети као уопштавање емпиријских закона гасовисавршеноуГаи-Луссац, Цхарлес и Боиле. Била је основна за проучавање идеалних гасова и омогућила је развој Термичке машине, чинећи их све ефикаснијим током последњих неколико деценија.
Погледајте такође: Открића физике која су се догодила несрећом
Цлапеиронова једначина: закон идеалног гаса
Цлапеиронова једначина је изведена из три емпиријска закона, односно закони који су утврђени експериментима. Такви закони објашњавају понашање гасова у трансформације гасаизоволуметријски (Гаи-Луссац закон), исобариц (Цхарлесов закон) и изотерме (Бојлов закон). Према овим законима:
у трансформацијама изоволуметријски, однос притиска и термодинамичке температуре идеалног гаса остаје константан;
у трансформацијама изобариц, однос запремине и термодинамичке температуре идеалног гаса је константан;
- у трансформацијама изотерме, производ притиска и запремине идеалног гаса остаје константан.
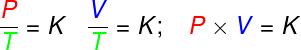
П. - притисак (Па - паскал)
В. - запремина гаса (м³)
Т. - термодинамичка температура гаса (К - келвин)
Из три горе наведена закона, Цлапеиронова једначина одређује која је вредност овога константан (К.) добијених у свакој од горе поменутих трансформација. Према Цлапеироновој једначини, ова константа је једнака броју молова помножених са а константа Р., позната као универзална константа идеалних гасова и једнака Болцманова константа множи Авогадров број.
Формула
Погледајте формулу која је позната као једначинауЦлапеирон:
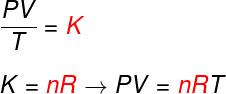
не - број молова (мол)
Р. - универзална константа идеалних гасова (Р = 0,082 атм.л / мол. К или 8,314 Ј.мол / К)
Анализирајући Цлапеиронову једначину, могуће је уочити да је притиска који врше идеални гасови је директно пропорционална температури а такође и да број мадежа. У наставку, притисак је обрнуто пропорционалан запремини заузета гасом.
О. модел идеалног гаса омогућено Цлапеироновом једначином широко се користи за развој машина које покреће течности, као што су машине на парни погон и мотори са унутрашњим сагоревањем.
Из Цлапеиронове једначине могло би се добити неколико важних резултата. На пример, један од њих предвиђа да 1 мол било ког идеалног гаса заузима запремину од 22,4 л када се подвргне притиску од 1 атм (1,01.105 Па) и на температури од 273К (0 ° Ц).
Погледајте такође: Најважнији концепти у термологији
Решене вежбе на Цлапеирон једначини
Питање 1 - (УЕЦЕ) Гас који може имати температуру, запремину и притисак повезани ПВ = нРТ има следеће карактеристике:
а) веома велика просечна удаљеност између молекула како би се занемариле интермолекуларне интеракције, осим када се сударају; молекули се подвргавају еластичним сударима.
б) врло мала средња удаљеност између молекула; молекули се подвргавају нееластичним сударима.
в) веома велика средња удаљеност између молекула како би се занемариле интермолекуларне интеракције, осим када се сударају; молекули се подвргавају нееластичним сударима.
г) веома велика средња удаљеност између молекула и са јаким интермолекуларним интеракцијама; молекули се подвргавају еластичним сударима.
Резолуција:
У моделу идеалног гаса, велики број бездимензионалних честица креће се великом брзином у случајним смеровима. Једине интеракције које трпе ове честице су савршено еластични судари, па је исправна алтернатива слово а.
Питање 2 - (УФРГС) Размотрите следеће изјаве о идеалним гасовима.
И. Константа Р присутна у једначини стања за гасове пВ = нРТ има исту вредност за све идеалне гасове.
ИИ. Једнаке запремине различитих идеалних гасова, при истој температури и притиску, садрже исти број молекула.
ИИИ. Просечна кинетичка енергија молекула идеалног гаса директно је пропорционална апсолутној температури гаса.
Који су тачни?
а) Само ја
б) Само ИИ
в) Само ИИИ
г) Само И и ИИ
д) И, ИИ и ИИИ
Шаблон:
Погледајмо алтернативе:
И. тачно, отуда се назива универзалном константом идеалних гасова.
ИИ. тачно. Према Цлапеироновој једначини, ако два идеална гаса имају исти притисак, температуру и запремину, тада је број честица у тим гасовима једнак.
ИИИ. тачно. Према теореми о енергетској еквивалентности, кинетичка енергија честица у идеалном гасу пропорционална је његовој температури.
Стога је исправна алтернатива слово е.
Питање 3 - (УФЈФ) Мушкарци попут Цлапеирон, Боиле, Мариотте, Гаи-Луссац, ван дер Валлс, између осталих, развили су важне студије које укључују својства гасова. Понашање стварних гасова приближава се идеалним гасовима у условима ниског притиска, као и гасовима садржаним у великој запремини и гасовима задржаним на високим температурама. Узмите у обзир да је у лабораторијском експерименту контејнер запремине В потпуно затворен и садржи 1 мол идеалног гаса под притиском 4,0 атм је подвргнут експанзији на константној температури која је једнака 127 º Ц и да се понашање овог гаса понаша као идеалан гас, као што је приказано у графика.
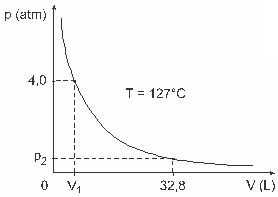
У овом случају, када гас заузима запремину једнаку 32,8 Л, притисак који врши на њега биће:
(Дато: универзална константа савршених гасова је Р = 0,082 атм. Л / мол. К.)
а) 0,32 атм
б) 0,40 атм
в) 1,0 атм
г) 2,0 атм
е) 2,6 атм
Резолуција:
Слово Ц.
Да бисмо решили вежбу, треба да применимо податке на Клапејронову једначину, али пре тога морамо температуру која је у степенима Целзијуса трансформисати у келвин. Провери:

Написао Рафаел Хеллербоцк
Наставник физике
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/fisica/a-equacao-clapeyron.htm
