Поларитет молекула је веома важан аспект, будући да су карактеристике супстанци, поред осталих фактора, одређене и чињеницом да су њихови молекули поларни или неполарни.
Одређивање поларитета молекула може се извршити помоћу Диполни момент или Резултат диполног момента, чији је симбол 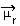 . Ако говоримо само о диполном моменту сваке везе у молекулу, онда је симбол грчко слово ми (µ).
. Ако говоримо само о диполном моменту сваке везе у молекулу, онда је симбол грчко слово ми (µ).

Молекул ће бити неполарни ако је диполни тренутак једнак нули, али ако је не-нула, значи да је поларни.

Постоје две важне ствари које треба узети у обзир при одређивању овог насталог диполног момента. Да видимо шта су:
1) разлика у електронегативности између атома елемената који учествују у реакцији. На пример, молекул ХФ има изразиту разлику у електронегативности, јер флуор привлачи, много више од водоника, пар електрона у вези. Дакле, расподела наелектрисања није симетрична, са електричним диполима.
Овај дипол је представљен вектором који је окренут ка крају који концентрише највише електрона, односно од најмањег до највише електронегативног атома. Дакле, у овом случају, вектор, који је једини, биће резултујући вектор, као што је назначено доле:
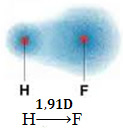
Имајте на уму да је векторска вредност једнака диполном тренутку, који је дат у дебие јединици (Д = 3,33. 10-30 цоуломб. Метро). Пошто диполни моменат није нула, молекул и веза јесу поларни.
Не заустављај се сада... После оглашавања има још;)
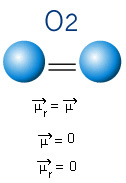
У молекулу испод имамо и молекул са само два атома, међутим, у овом случају он одговара једноставној супстанци, односно састоји се од само једне врсте елемента. Према томе, нема разлике у електронегативности; атоми такође привлаче електроне који су симетрично распоређени. Добијени диполни момент једнак је нули, па су и веза и молекул аполар.
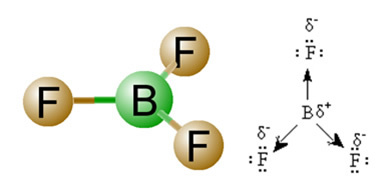
2) Геометрија молекула, односно просторни распоред вектора. Молекул БФ3 има три поларне везе, у којима је флуор најелектронегативнији, па вектори усмерени ка њему. Међутим, с обзиром да је просторни распоред атома раван тригонално, то чини електроне симетричним распоредом око централног атома. Дакле, резултат је да се ова три вектора међусобно поништавају и да је диполни тренутак једнак нули. Према томе, молекул БФ3 é аполате.
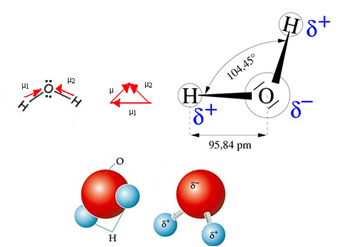
Молекул воде има два вектора, међутим, његова просторна геометрија није равна, већ у облику В. На следећој слици имајте на уму да се на овај начин њихови вектори међусобно не искључују, електрони се дистрибуирају асиметрично и концентришу се у најелектронегативнијем атому, а то је кисеоник. Дакле, диполни моменат се разликује од нуле, а молекул воде је поларни:
Јеннифер Фогаца
Дипломирао хемију