ТХЕ Електрохемија је грана Физичке хемије која проучава реакције у којима постоји пренос електрона (реакције окси-редукције) и његове претварање у електричну енергију, као и супротан процес, односно претварање електричне енергије у енергију хемија.
Први процес је оно што се одвија у Батерије. Батерије су уређаји формирани од две електроде (позитивни пол, која је катода, и негативни пол, која је анода), поред електролита (проводни раствор). Електрони се спољним проводником преносе са аноде на катоду, формирајући електричну струју која се користи за укључивање неког уређаја. Батерије се састоје од неколико ћелија повезаних серијски или паралелно.
Ово је спонтан процес и енергија се испоручује све док се хемијска реакција не исцрпи (као што је случај са примарним ћелијама и батеријама, попут Лецланцхеове суве ћелије и батерије алкална), или, у случају реверзибилних реакција, може се применити разлика потенцијала и реакција се обрнути, поново формирајући реактанте и допуњавајући батерију која спреман је за поновну употребу (ово је случај батерија и секундарних батерија, као што су олово, које се користе у аутомобилима и литијум-јони, које се користе у уређајима мобилни телефони).

Примарне ћелије и батерије у првом плану, а у другом пуњење секундарних батерија (оловних и литијумових јона)
Обрнути процес није спонтан и назива се електролиза. Електролиза је пролазак електричне струје која долази из генератора, попут ћелије или батерије, кроз јонску течност. Ако је течност нека растопљена супстанца, имамо а магматска електролиза, али ако је то водени раствор, имамо водена електролиза.
Приликом проласка електричне струје преко течног медија, генератор „извлачи“ електроне са позитивног пола (анода - она је супротна од батерија) електролитске ћелије и преноси их на негативни пол (катоду), односно катода пролази кроз редукцију, а анода оксидација. Тако се електрична енергија коју испоручује генератор трансформише у редокс реакције (хемијска енергија). Испод је шема електролизе воде:
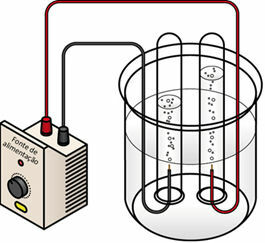
Шема електролизе воде
Електролиза се широко примењује индустријски у производњи важних супстанци, као што су алуминијум, гасовити хлор, метални натријум, и за пречишћавање или заштиту различитих метала, као у поступцима галванизације или галванизације, који се састоје у пресвлачењу неког предмета металом, као што је посребрење, бакарисање, никловање, позлата и хроматизација; када је челик обложен цинком, то се назива поцинчавање.
У одељку од Електрохемија на нашој веб страници ћете пронаћи више детаља о свим аспектима који се односе на ћелије и батерије, као и на електролизу.
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eletroquimica.htm

