
Количина калорија зависи од конституције хране. Дакле, да бисмо експериментално утврдили количину топлоте коју ослобађа храна и коју тело може да апсорбује, користимо уређај тзв. калориметар.
Овај уређај мери топлоту која се ослобађа од хране приликом сагоревања. Постоји неколико врста калориметара; први од њих створили су 1780. године Лавоазије и Лаплаце и био је ледени калориметар.
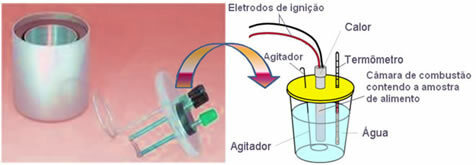
Данас се највише користи и узима у обзир горе објасњени концепт калорија водени калориметар. Овај уређај је прекривен изолационим материјалом да би се спречио губитак топлоте из медија; а храна која се анализира ставља се у комора за сагоревање, који садржи гас кисеоника и електроде. Ове електроде се подвргавају електричном пражњењу и узрокују њихово паљење и сагоревање хране.
Позната маса воде садржана у калориметру апсорбује топлоту коју ослобађа сагорела храна и а термометар мери пораст температуре воде. Поред тога, калориметар садржи а агитатор што омогућава да температура воде у целости остане једнолична.
Тако, ако користимо, на пример, масу од 1 грама шећера, а калориметар има 1000 г воде и примећујемо да на крају реакције, температура воде је прешла са 20 ° Ц на 24 ° Ц, односно повећала се за 4 ° Ц, тада можемо постићи енергетску вредност шећер. Као? Па, с обзиром на почетни концепт калорија, имамо:
| Повећати са 1 ° Ц → 1 кал на грам воде |
| Подигните са 4 ° Ц → 4 кал по граму воде |
Дакле, 1 г воде упије 4 креча. Међутим, употребљено је 1000 г воде и, с обзиром на то да је она апсорбовала сву топлоту која се ослобађа у сагоревању, укупна енергија коју је вода упила била је 4000 цал или 4 кцал. Стога закључујемо да:
| Енергетска вредност шећера = 4000 кал / г или 4 кцал / г. |
Претварање у СИ:
1 кцал 4,18 кЈ
4 кцал / г к
к = 16,72 кЈ / г
Поред тога, можемо да користимо следећу једначину за израчунавање количине топлоте која се предаје или апсорбује водом:
| К = м. ц. т |
Где:
К = топлота која се предаје или апсорбује водом;
м = маса воде;
ц = специфична топлота воде, која је једнака 1,0 кал / г. ° Ц или 4,18 Ј / г. ° Ц;
Δт = варијација температуре коју трпи вода, а која се даје смањењем коначне температуре за почетну (тф - ти).
Користећи ову формулу добијамо исти резултат:
К = м. ц. т
К = 1000 г. 1,0 кал / г. ° Ц. (24-20) ° Ц
К = 4000 кал
К = 4,0 кцал
или
К = м. ц. т
К = 1000 г. 4,18 кЈ / г. ° Ц. (24-20) ° Ц
К = 16,72 кЈ
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/medindo-as-calorias-dos-alimentos-por-meio-um-calorimetro.htm
