Горива која се користе у већини аутомобила су бензин и етанол. Потпуно сагоревање ова два горива ствара угљен-диоксид (ЦО2 (г)) и воде (Х.2О). Нажалост, непотпуно сагоревање и нечистоће присутне у алкохолу и бензину могу створити супстанце које веома загађују животну средину. У случају бензина, угљен моноксид (ЦО(г)); угљоводоници (једињења која се састоје од угљеника и водоника), као што је етан (Ц.2Х.6 (г)); и оксиди азота (НОИкс), углавном азот моноксид (НО) и азот диоксид (НО2 (г)).
Дакле, да би се избегло повећање загађења ваздуха, свим аутомобилима је потребна опрема која се зове каталитички претварач или каталитички претварач, који је уређај против загађења, који има функцију обраде ових гасова које ослобађа мотор са унутрашњим сагоревањем и њихове трансформације у мање штетне гасове. У ту сврху се у неким индустријским процесима користе и катализатори.
Поменути загађујући гасови напуштају мотор и улазе у катализатор, пролазећи кроз неку врсту "кошнице", чије су ћелије углавном направљене од керамичког или металног материјала, који је обложен глиницом (алуминијум-оксид - Ал
2О.3). Овај облик саћа, са сићушним каналима, важан је јер пружа велику контактну површину гасовима, чинећи их бржом реакцијом.Али прави катализатор је метал који се налази на врху алуминијумског оксида. Обично се користе метали паладијум, родијум, платина или молибден. Такође можете мешати ове метале и користити легуре. На пример, у случају бензина, обично се користи легура паладијума и торијума; у случају етанола користи се друга легура паладијума и молибдена. Ови метали врше хетерогену катализу са загађујућим гасовима.
хетерогена катализа то је врста реакције у којој катализатор са реактантима (у овом случају загађујућим гасовима) формира полифазни систем. То је зато што се катализатор адсорбује, односно задржава молекуле реактаната на својој површини, слабећи њихове везе и убрзавајући процес реакције.
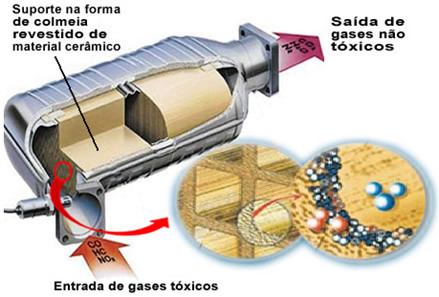
Као резултат, метали катализатора трансформишу загађиваче попут ЦО и НОИкс у нетоксичним гасовима као што је ЦО2, Х2О, О2 и без2. Погледајте неке од ових реакција у наставку и приметите да кроз њих долази до оксидације угљоводоника и ЦО (добијен непотпуним сагоревањем), а такође и редукција азотних оксида у гас азота (Н2):
2 ЦО(г) + 2 НЕ(г) → 2 ЦО2 (г) + 1 Н.2 (г)
2 ЦО(г) + 1 О.2 (г) → 2 ЦО2 (г)
2Ц2Х.6 (г) + 7 О.2 (г) → 4 ЦО2 (г) + 6 Х.2О.(в)
2 НЕ2 (г) +4 ЦО(г) → 1 Н.2 (г) + 4 ЦО2 (г)
2 НЕ2 (г) → 1 Н.2 (г) + 2 О.2 (г)
2 НЕ(г) → 1 Н.2 (г) + 1 О.2 (г)
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/conversor-catalitico.htm


